
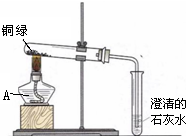
 铜器长期暴露在空气中会生成铜绿(俗称铜锈).为探究铜锈的组成,小明在老师的指导下,按图装置进行实验:
铜器长期暴露在空气中会生成铜绿(俗称铜锈).为探究铜锈的组成,小明在老师的指导下,按图装置进行实验:

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
 30、据媒体报道,2009年2月12日我外交部发言人就法国佳士得公司拍卖我圆明园兔首和鼠首两件文物(如右图),发表严正声明:中国对其拥有不可置疑的所有权.这两件文物均为青铜器,其表面呈绿色,这是铜器长期暴露在空气中生锈的结果.晓航对铜器生锈的条件产生了兴趣.
30、据媒体报道,2009年2月12日我外交部发言人就法国佳士得公司拍卖我圆明园兔首和鼠首两件文物(如右图),发表严正声明:中国对其拥有不可置疑的所有权.这两件文物均为青铜器,其表面呈绿色,这是铜器长期暴露在空气中生锈的结果.晓航对铜器生锈的条件产生了兴趣.
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 ”为铜片):
”为铜片):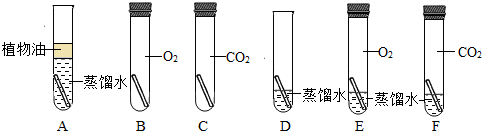
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g?cm-3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
| 实验步骤 | 观察到的现象 |
| ①在试管中取少量盐酸,插入铁丝,充分作用. | |
| ②在①所得的溶液中,插入 铜丝 铜丝 ,充分作用. |
无明显现象 |
| ③在②所得的溶液中插入 铝丝 铝丝 ,充分作用. |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g?cm-3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com