
����ʡ�ѽ���Сѧ����ѧ��������γ̼ƻ���������ѧ���е�ѧ�������Ҫ������ѧ�仯����

A. �ɼ�����걾 B. ����ӣ�� C. ����� D. ̿�����
D ��������A���ɼ�����걾������û�����������ɣ����������仯���ʴ���B������ӣ��������û�����������ɣ����������仯���ʴ���C����ֲ���������û�����������ɣ����������仯���ʴ���D��̿����������������ʶ�����̼���ɣ����ڻ�ѧ�仯������ȷ����ѡD�� ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ʡ�˲���2018���п���ѧ�Ծ� ���ͣ���ѡ��
NaNO2�е�Ԫ�صĻ��ϼ���( )
A. -3 B. +2 C. +3 D. +4
C �����������ݻ������л��ϼ������ܼ۴�����Ϊ��ԭ��NaNO2�е�Ԫ�صĻ��ϼ��ǩv+1�w��x���v-2�w��2��0,x��+3����ѡC���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ2018���п���ѧ�Ծ� ���ͣ������
ѡ�������������(�����)���پƾ� ������� �۾���ϩ �ܺϳ���
(1)���������Ϸʵ���_____�� (2)������ȼ�ϵ���_____��
(3)����������̥����_____�� (4)��������ʳƷ��װ������_____��
�� �� �� �� �������� (1)��������м�Ԫ�غ͵�Ԫ�أ�������ڸ��Ϸʣ�(2)�ƾ����п�ȼ�ԣ��������ȼ�ϣ�(3)�ϳ�������������̥��(4) ����ϩ���Ͽ���������ʳƷ��װ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ��ҵ�������������ѧ�Ծ� ���ͣ�������
ij��������������(��Ҫ��FeO��Fe2O3������һ������SiO2)����������ˮ��������������(FeSO4•7H2O)���乤���������£�

�������ϣ�SiO2������ˮ��Ҳ����ϡ���ᷴӦ��
(1)����ȡ�������У�FeO��Fe2O3��ϡ���ᷢ����Ӧ�Ļ�ѧ����ʽ�ֱ�ΪFeO+H2SO4=FeSO4+H2O��________��
(2)Ϊ��ߡ���ȡ������ķ�Ӧ���ʣ��ɲ�ȡ�ľ����ʩ��________(дһ���������ǡ����衱�͡�ʹ�ô�����)��
(3)����ԭ�������Ŀ���ǽ�Fe3+ת��ΪFe2+���Լ�X����SO2��Fe�����Լ�X��Fe��ת��ԭ��ΪFe+Fe2(SO4)3=3FeSO4����á���ԭ������Һ��pH����������ԭ����________��
(4)��FeSO4��Һ�õ�FeSO4•7H2O�Ĺ����а���������________�Ȳ�����������������������IJ��������оƾ��ơ�________��
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O ���������Ũ�ȡ������¶ȡ������������ �����Ĺ��������ᣬ��Һ���Լ��� �ᾧ ������ ��������(1)����ȡ�������У�FeO��Fe2O3��ϡ���ᷢ����Ӧ�Ļ�ѧ����ʽ�ֱ�Ϊ��FeO+H2SO4=FeSO4+H2O��Fe2O3+3H2SO4=Fe2(SO4)3+3H2O��(2)Ϊ��ߡ���ȡ������ķ�Ӧ���ʣ��ɲ�ȡ�ľ����ʩ�У����������Ũ�ȣ�...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ��ҵ�������������ѧ�Ծ� ���ͣ���ѡ��
ѧϰ��ѧ����Ҫ�����ǽ���ģ�͡������й�ģ�ʹ������
A.  ʯī�ṹģ�� B.
ʯī�ṹģ�� B. 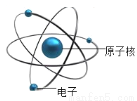 ԭ�ӽṹģ��
ԭ�ӽṹģ��
C.  ���ʷ���ģ�� D.
���ʷ���ģ�� D.  ��Һ����ģ��
��Һ����ģ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ��Ӫ��2018���п���ѧ�Ծ� ���ͣ������
�ҹ���ѧ�Һ�°����ĺ����ƼΪ���ҵ�����ķ�չ�����˽ܳ��Ĺ��ס����Ʊ�����Ĺ������漰Na2CO3��NaCl��NH4Cl��NaHCO3�����ʡ����ϱ������ݻش��������⣺
�¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ��/g | Na2CO3 | 7 | 12.2 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 |
(1)�������������У��ܽ������ڿ��ܵ�������__________��
(2)��50��ʱ����100gˮ�м���48gNa2CO3��ֽ���������Һ����Ϊ___________ �������ձ��и������������䣬������40��ʱ��������Һ���ʵ�����������_________(���С���������䡱���)��
(3)����ݱ��������ݣ�����ͼ�л��Ƴ�̼���Ƶ��ܽ�����ߡ�
 __________
__________
(4)�����ܽ�����ش��������⣺
��60��ʱ������������������ֹ��������зֱ��ˮ��ɱ�����Һ��������Һ�����ɴ�С��˳����_____________________________��
�ں����Ƽ�Ĺؼ������ǣ�����ʳ��ˮ��ͨ�백�����Ƴɱ��Ͱ���ˮ������ˮ���ն�����̼������̼�����ƺ��Ȼ�泥��仯ѧ����ʽΪNaCl+NH3��H2O+CO2��NH4Cl��NaHCO3���������ɵ�̼�����ƺ��Ȼ�泥�����������������______________��������_________________��
̼������(��NaHCO3) 147.3g ��� NaHCO3��NaCl��Na2CO3��NH4Cl(��NaHCO3��NaCl��Na2CO3��NH4Cl) ̼������(��NaHCO3) NaHCO3���ܽ��ԶС��NH4Cl���ܽ��(��NaHCO3���ܽ�Ƚ�С����Ӧ���ɵ�̼���������������Ȼ�泥�����ͬ�¶���NaHCO3���ܽ��ԶС��NH4Cl���ܽ��) �����������⿼���˴������ȡ���ܽ������Ӧ��...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ��Ӫ��2018���п���ѧ�Ծ� ���ͣ���ѡ��
�����(C4H9Li)���ϳɹ�ҵ��һ�ֳ��õ��Լ�����ɫ��ĩ���۵�-95�棬�е�80�棬��ˮ������������ȼ�����й��ڶ���﮵�˵����ȷ����
A. ���������4��̼ԭ�ӡ�9����ԭ�ӡ�1���ԭ�ӹ��ɵ�
B. �������̼Ԫ����������Ϊ75%
C. ����������ʹ�ù������������ȼ�գ�������ˮ����
D. ��������л��߷��ӻ�����
B ��������A����������ɷ��ӹ��ɵģ�������ԭ��ֱ�ӹ��ɵģ�����B���������̼Ԫ����������=��100%=75%����ȷ��C���������ˮ����ȼ���������ʹ�ù������������ȼ�գ�������ˮ���𣬴���D���л��߷��ӻ��������Է�����������������ʮ����﮵���Է�������Ϊ12��4+1��9+7=64���������л��߷��ӻ��������ѡB���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������к�����2018����꼶��ο���ѧ�Ծ� ���ͣ���ѡ��
��ȥ���и����ʣ���Һ���е��������ʣ����÷������е���
ѡ�� | ���� | �������� | ��ȥ���ʵķ��� |
A | NaNO3 | Na2CO3 | ������ϡ���ᣬ�����ᾧ |
B | Cu(NO3)2 | AgNO3 | ��������ͭ�ۣ���ַ�Ӧ����� |
C | NaCl | Na2SO4 | ��������BaCl2��Һ����ַ�Ӧ����ˣ�ϴ�ӣ����� |
D | CaCl2 | HCl | ��������CaCO3��ĩ����ַ�Ӧ����� |
A. A B. B C. C D. D
BD ��������A������������ϡ����������ᾧ�������Ȼ����������룬�ʴ��� B��������������ͭ��Ӧ��������ͭ���������˳�ȥ���壬���ɻ������ͭ��Һ������ȷ�� C���Ȼ����л��������ƣ���������BaCl2��Һ����ַ�Ӧ����ˣ�ϴ�ӣ�����õ��������ᱵ��������Ӧ���ǽ���Һ�����ᾧ���ʴ��� D��ϡ���������̼��Ʒ�Ӧ�����Ȼ��ƺͶ�����̼���ʿ��Գ�ȥ���ʣ��Ҳ������µ����ʣ�����ȷ��...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ��ׯ��ỳ���2018����꼶��ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ʵ����
��ͼΪʵ���ҳ��õ�ʵ��װ�ã���ش����⡣

��1����װװ����ϣ�װҩƷǰҪ__________������BCװ�������ȡ������ʵ���й۲쵽ˮ��������____________________ʱ����ʼ�ռ���
��2������������һ�־�����Ⱦ�Ե����壬ʵ�������������ƹ����Ũ��������ȡ������и÷�Ӧ��ѡ�õķ���װ����__________������ĸ�����ռ���������ѡ�õ���Fװ�ã���˿�֪����������ܶ�__________������ڡ�����С�ڡ����ڡ����������ܶȣ�Fװ���е�����������ҺҪ���������������û�ѧ����ʽ��ʾ____________________���÷���ʽ��ʾ��
���װ�õ������� �������ȳ��� B ���� SO2+2NaOH=Na2SO3+H2O ��������������Ҫ�����˳�������ķ���װ�ú��ռ�װ����ѡȡ��������ȡ�����IJ��������ע��㡣�������ȡװ�õ�ѡ���뷴Ӧ���״̬�ͷ�Ӧ�������йأ�������ռ�װ�õ�ѡ����������ܶȺ��ܽ����йء� ��1����װװ����ϣ�Ϊ�˱����ռ�����������ռ��������岻����װҩǰҪ�ȼ��װ�õ������ԣ���ˮ���ռ�����ʱ��Ҫ������...�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com