
下列物质放入水中温度会下降的是 ( )
A. 生石灰 B. 硝酸铵 C. 氯化钠 D. 浓硫酸
B 【解析】A. 生石灰即氧化钙和水反应放出大量的热,错误。 B. 硝酸铵溶于水温度降低,正确; C. 氯化钠溶于水没有明显的温度变化,错误; D. 浓硫酸溶于水放出大量热,错误。故选B。 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:初中化学 来源:吉林省长春市宽城区2018届九年级第一次模拟测试化学试卷 题型:填空题
请回答下列与金属有关的问题。
张同学验证金属的活动性顺序时,向CuCl2和FeCl2的混合溶液中加入一定量的Zn粉,发现溶液颜色逐渐变成了无色。
(1)这一现象证明Zn的金属活动性比铁和铜_______(选填“强”或“弱”);
(2)写出上述变化过程中的一个反应方程式______,此反应的基本类型是_______反应;
(3)要进一步验证铁和铜的活动性,可选用的试剂是_________。
强 Zn+CuCl2==Cu+ZnCl2 置换 铁丝和CuCl2 溶液 【解析】向CuCl2和FeCl2的混合溶液中加入一定量的Zn粉,锌比铁和铜活泼,铁比铜活泼,活泼金属可以置换不活泼金属,溶液颜色逐渐变成了无色,氯化锌溶液无色。(1) 溶液颜色逐渐变成了无色,氯化锌溶液无色,证明Zn的金属活动性比铁和铜强,氯化铜溶液和氯化亚铁溶液均有色。(2)变化过程中的一个反应方程式是Zn+CuCl2...查看答案和解析>>
科目:初中化学 来源:安徽省长丰县2018届九年级下学期第二次教学质量检测化学试卷 题型:科学探究题
化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。各小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末。
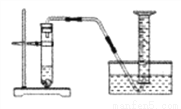
A组:探究催化剂对化学反应速率的影响;
取5mL10%H2O2溶液,三次实验分别加人0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
试剂 | MnO2 | 红砖粉末 | CuO |
t/s | 10 | 60 | 20 |
由此得出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用。
(1)你认为该结论是否正确,为什么?_________________________________________。
(2)经过补充对比实验,证明红砖粉末有催化作用,则三者的催化效率由高到低的顺序为___________。
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,,进行实验,记录时间t1。
(3)乙同学:取10mL2.5%H2O2溶液,加入__________为催化剂,进行实验,记录时间t2。
实验结果:_______________________________________________________
结论:___________________________________________________________
【拓展探究】
(4)C组:探究____________对化学反应速率的影响。
各取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴,记录时间t3、t4。
(5)实验结果:_________________________;
结论:当反应物浓度和催化剂相同时,__________________________________。
(6)以上三组实验说明,影响化学反应速率的因素有:________________________。
不正确,无法比较加入红砖粉末后过氧化氢的分解速率与不加红砖粉末时过氧化氢的分解速率的大小 相同条件下,H2O2的浓度越大,分解速率越大 温度 温度越高,分解速率越大 催化剂、浓度、温度 【解析】(1)无法比较加入红砖粉末后过氧化氢的分解速率与不加红砖粉末时过氧化氢的分解速率的大小。(2)收集相等体积的氢气,所用时间越短,说明化学反应速率越快。(3)做对比实验,必须控制变量,当只有一个条件不同...查看答案和解析>>
科目:初中化学 来源:江苏省江阴市2018届九年级下学期期中考试化学试卷 题型:填空题
2018年3月5日台湾民进党政府宣布重启核电,而台湾是个地震多发的地区,可能重蹈2011年日本大地震引发重大核事故,并不顾民意的反对欲开放来自日本核灾地区的食品。
(1)核电站中核燃料铀或钚在中子的撞击下,原子核发生分裂,产生钡、氙、碘、铯、锶等原子和一些粒子及射线,同时释放大量的能量,这些能量可用于驱动汽轮机发电。从物质的变化上看,核变化与化学变化的相同点是___________________________;从原子的变化上看,核变化与化学变化的不同点是____________________。
(2)地震发生后因断电海水冷却系统停止工作,反应堆温度过高使水蒸气与钢壳反应生成四氧化三铁和氢气,该反应的化学方程式是____________________。
(3)高温条件下氢气和空气混合爆炸,这一爆炸过程属于_____(填“物理”或“化学”)变化。爆炸引起核泄漏,造成铯137(137是相对原子质量)散逸到空气中。铯的核电荷数是55,则铯的中子数是_______。
(4)下列说法错误的是__________。
A.科学、安全地利用核能 B.充分利用风能、地热能和太阳能
C.尽可能多使用石油、煤等化石能源 D.寻找可循环利用的生物能源
都产生新物质 核变化原子发生了变化(原子核发生了变化)而化学变化原子本身没有发生变化(原子核没有变) 4H2O+3Fe Fe3O4+4H2, 化学 82 C 【解析】有新物质生成的变化叫化学变化;金属是由原子直接构成。铀或钚在中子的撞击下,原子核发生分裂,产生钡、氙、碘、铯、锶等原子,说明产生了金属钡等新的物质,从物质的变化上看,核变化与化学变化的相同点是都产生新物质;从原子的变化上看,核变...查看答案和解析>>
科目:初中化学 来源:江苏省江阴市2018届九年级下学期期中考试化学试卷 题型:单选题
下列选用的除杂试剂和实验操作都正确的是(括号内为杂质) ( )
选项 | 物质 | 除杂试剂(足量) | 操作方法 |
A | CO2(HCl) | 氢氧化钠溶液 | 气体通过盛有氢氧化钠溶液的洗气瓶 |
B | NaCl(Na2CO3) | 盐酸 | 加入足量盐酸、蒸发、结晶 |
C | MnO2(NaCl) | 水 | 加入足量水溶解、过滤、洗涤、干燥 |
D | Cu(CuO) | 氧气 | 通入足量氧气并加热 |
A. A B. B C. C D. D
BC 【解析】除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.A氢氧化钠和二氧化碳反应,不符合除杂的要求;盐酸和杂质碳酸钠反应生成氯化钠和水、二氧化碳,反应后的溶液中的溶质一定有氯化钠,可能会有少量剩余的氯化氢,蒸发结晶可将水,氯化氢全蒸发掉,只得氯化钠晶体,符合除杂要求;B二氧化锰不溶于水,而氯化钠易溶于水,加水后过滤,可将二氧化锰与氯化...查看答案和解析>>
科目:初中化学 来源:北京市海淀区2018年九年级第二学期期中练习 题型:简答题
小明同学用下图所示装置进行实验。甲瓶中充满二氧化碳气体,注射器中装有氢氧化钠浓溶液,乙中盛有足量稀盐酸。小明先关闭止水夹,然后将氢氧化钠浓溶液全部注入甲瓶,一段时间后再打开止水夹。
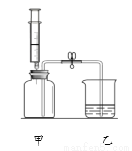
(1)注入氢氧化钠浓溶液后,甲中发生反应的化学方程式为_____________。
(2)打开止水夹,可观察到的现象有_____________、_____________。
2NaOH + CO2Na2CO3 + H2O 乙中液体倒吸入甲中, 甲中产生无色气体 【解析】(1)氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,反应方程式为2NaOH + CO2Na2CO3 + H2O ; (2)由于氢氧化钠与二氧化碳反应,使瓶内的气体含量减少,内压将低,故打开止水夹后,有液体倒流溶液集气瓶中,流入的稀盐酸与生成的碳酸钠反应,生成二氧化碳气体,故又可以看到有无色气体产...查看答案和解析>>
科目:初中化学 来源:北京市海淀区2018年九年级第二学期期中练习 题型:简答题
从1世纪起,铁便成了一种最主要的金属材料。

(1)上述三种铁矿石的主要成分属于氧化物的是__________。
(2)工业上用一氧化碳和赤铁矿炼铁的原理是__________(用化学方程式表示)。
Fe2O3、Fe3O4 (或写氧化铁、四氧化三铁等物质名称) Fe2O3 + 3CO 2Fe + 3CO2 【解析】(1)赤铁矿和磁铁矿中的主要成分是氧化物,分别是Fe2O3、Fe3O4; (2)工业上用一氧化碳与氧化铁在高温的条件下反应生成铁和二氧化碳,反应方程式为Fe2O3 + 3CO 2Fe + 3CO2查看答案和解析>>
科目:初中化学 来源:重庆市江津区2018届九年级下学期六校联考化学试卷 题型:实验题
化学是一门以实验为基础的科学,请根据下列所示的示意图回答问题。
(1)实验1中,集气瓶内进入水的体积约为集气瓶中空气总体积的___________。
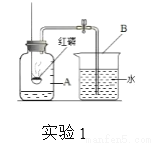
(2)实验2中,把干燥的紫色石蕊纸花和湿润的紫色石蕊纸花分别伸入两瓶干燥的二氧化碳气体中,可以观察到_________(填“干燥的紫色石蕊纸花”或“湿润的紫色石蕊纸花”)变红的现象,则其变红原因是____(请用化学方程式表示)。
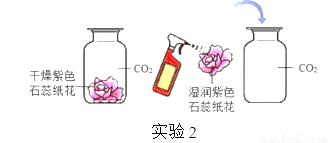
(3)实验3中,若B处盛放木炭,分别进行以下操作:Ⅰ.先在A处通入氮气一段时间后,再在B处加热,B、C处没有明显变化;Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊。则Ⅱ与Ⅲ对比,说明物质燃烧的条件之一是____________。

(4)实验3中,若B处盛放氧化铁粉末,分别进行以下操作:先在A处通入一氧化碳,一段时间后,再在B处的下方通过使用酒精喷灯获得高温,B处可以观察到红色粉末逐渐变黑的现象,发生反应的化学方程式为________。
1/5; 湿润的紫色石蕊纸花; CO2+H2O==H2CO3 ; 需要达到可燃物的着火点 3CO + Fe2O32Fe + 3CO2 【解析】(1)测定空气中氧气含量的原理是,利用物质与空气中的氧气反应,又不生成气体,使瓶内气体减少,压强变小,水倒流入集气瓶内,倒流的水的体积就等于瓶内氧气的体积。氧气约占空气体积的五分之一,故实验1中,集气瓶内进入水的体积约为集气瓶中空气总体积的五分之一;(...查看答案和解析>>
科目:初中化学 来源:广州市白云区2018届九年级中考一模化学试卷 题型:单选题
某气体只能用排水法收集(下图),下列说法正确的是
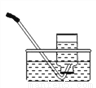
A. 当导管口开始有气泡冒出时立即收集
B. 当集气瓶口冒出大量气泡时停止收集,取出,再用玻璃片粗糙面盖上
C. 当集气瓶口冒出大量气泡时停止收集,在水下用玻璃片光滑面盖上, 取出
D. 该气体具有的性质是:不易(或难溶于水);密度与空气接近或与空气中的成分反应
D 【解析】A. 当气泡连续均匀冒出时开始收集气体,错误;B. 当集气瓶口冒出大量气泡时停止收集,用玻璃片粗糙面盖上集气瓶,然后将集气瓶连同玻璃片一起取出,错误;C. 当集气瓶口冒出大量气泡时停止收集,在水下用玻璃片粗糙面盖上,取出,错误;D. 由于该气体只能用排水法收集,则该气体不易(或难溶于水),其密度与空气接近或与空气中的成分反应,正确。故选D。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com