
| A. | 50% | B. | 74.2% | C. | 96.4% | D. | 94.6% |
分析 根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,依据二氧化碳的质量计算样品中碳酸钠的质量,碳酸钠和氢氧化钙反应生成氢氧化钠和碳酸钙,依据固体质量的变化计算碳酸钠的质量,然后计算碳酸钠的含量.
解答 解:设与盐酸反应的碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{x}$=$\frac{44}{2.2g}$
x=5.3g
设碳酸钠与氢氧化钙反应生成碳酸钙沉淀的质量为y
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 100
5.3g y
$\frac{106}{5.3g}$=$\frac{100}{y}$
y=5g
所以混合物中杂质的质量为10.3g-5g=5.3g
所以纯碱样品中Na2CO3的含量是:$\frac{5.3g}{5.3g+5.3g}$×100%=50%,故选:A.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:初中化学 来源: 题型:填空题
 人类的生活和工农业生产都离不开水.
人类的生活和工农业生产都离不开水.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/ | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
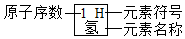
| 1H 氢 | 2He 氦 | |||||||
| 3Li 锂 | 4Be 铍 | 5B 硼 | 6C 碳 | 7N 氮 | 8O 氧 | 9F 氟 | 10Ne 氖 | |
| ll Na 钠 | 12Mg 镁 | 13A1 铝 | 14Si 硅 | 15P 磷 | 16S 硫 | X C1 氯 | 18Ar 氩 | |
| 19K 钾 | 20Ca 钙 | … | ||||||
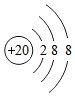 表示的是Ca2+(写粒子的符号)
表示的是Ca2+(写粒子的符号)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳、氢、氮三种元素的原子个数比为3:4:1 | |
| B. | 对苯二胺是由6个碳原子、8个氢原子和2个氮原子构成 | |
| C. | 对苯二胺由碳、氢、氮三种元素组成 | |
| D. | 对苯二胺中碳、氢、氮元素质量比为18:2:7 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 事实 | 解释 | |
| A | 搜救犬搜索到幸存者 | 分子是运动的 |
| B | 双氧水能杀菌消毒而水则不能 | 两种物质的分子构成不同 |
| C | 100mL酒精和100mL水混合在一起,体积小于200mL | 分子很小 |
| D | 加热氧化汞可得到金属汞和氧气 | 分子是可以再分的 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com