
【题目】某工厂产生的废渣(主要含![]() 、
、![]() ,还有一定量的
,还有一定量的![]() )可用于制备硫酸亚铁晶体,其工艺流程如下:(查阅资料:
)可用于制备硫酸亚铁晶体,其工艺流程如下:(查阅资料:![]() 不溶于水和酸。)
不溶于水和酸。)
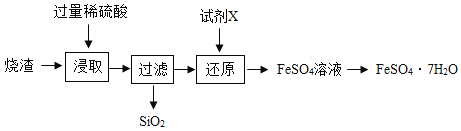
(1)“浸取”步骤中![]() 与硫酸反应生成硫酸亚铁和水,写出反应的化学方程式为_______;
与硫酸反应生成硫酸亚铁和水,写出反应的化学方程式为_______;
(2)“浸取”步骤中常常将废渣粉碎、搅拌或提高硫酸浓度,目的都是____________;
(3)“还原”步骤的目的是将![]() 转化为
转化为![]() ,“试剂”可选用下列两种物质:
,“试剂”可选用下列两种物质:
①若试剂X是![]() 转化原理:
转化原理:![]() ,则Y的化学式为________;
,则Y的化学式为________;
②若试剂X是![]() 转化原理:
转化原理:![]() ,测得还原后的溶液pH增大,其原因是:
,测得还原后的溶液pH增大,其原因是:
A ![]() 和过量的硫酸反应 B ________________________
和过量的硫酸反应 B ________________________
【答案】![]() 加快反应速率
加快反应速率 ![]()
![]() 的酸性没有
的酸性没有![]() 强(合理给分)
强(合理给分)
【解析】
(1)氧化亚铁和硫酸反应生成硫酸亚铁和水,化学方程式为:FeO+H2SO4=FeSO4+H2O;
(2)“浸取”步聚中常常将废渣粉碎、搅拌或提高硫酸浓度,目的都是:加快反应速率;
(3)由反应的化学方程式可知,反应前后硫原子都是4个,铁原子都是2个,反应后的氧原子是16个,反应前应该是16个,其中2个包含在2Y中,反应后氢原子是4个,反应前应该是4个,都包含在2Y中,所以Y是H2O;
若试剂X是Fe转化原理; Fe+Fe2 (SO4)3=3FeSO4,测得还原后的溶液pH增大,其原因是:
A Fe 和过量的硫酸反应
B 硫酸亚铁的酸性没有硫酸铁强。
故答案为:(1)FeO+H2SO4=FeSO4+H2O;
(2)加快反应速率;
(3)H2O;硫酸亚铁的酸性没有硫酸铁强。


科目:初中化学 来源: 题型:
【题目】在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入100g溶质质量分数为73%的稀盐酸,天平呈平衡状态。然后向左、右两盘的烧杯中分别加入下列各物质,充分反应后,天平指针不会发生偏转的是(不考虑稀盐酸的挥发)( )
A.10g碳酸钙和10g碳酸钠B.8.4g碳酸氢钠和8.4g碳酸镁
C.1.8g铝粉和1.8g锌粉D.4.6g氧化铁粉末和4.8g镁条
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁元素的相关信息如图所示,下列有关铁的说法正确的是( )
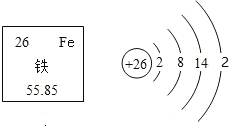
A.相对原子质量为55.85g
B.属于人体必需的常量元素
C.原子的核电荷数、质子数、电子数都为26
D.在化学变化中容易失去最外层电子形成Fe+2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某碱厂年产纯碱120万吨,它的产品除了纯碱外,还有氯化钙和碳酸氢钠。该厂生产纯碱的工艺流程可简单表示如下:
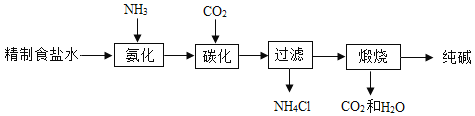
其生产过程中涉及的主要化学反应有:①NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓;②2NaHCO3![]() Na2CO3+ CO2↑+ H2O。
Na2CO3+ CO2↑+ H2O。
请回答:
(1)①“碳化”过程中需要的CO2,可由石灰石高温煅烧得到,该反应的化学方程式为__________。
②实验室中,通常用稀盐酸与石灰石反应制取CO2气体,不选用浓盐酸的理由是_____________;干燥CO2气体,可用的干燥剂是_________(填字母)。
A浓硫酸 B固体氢氧化钠 C生石灰
(2)①该厂“过滤”所得的NH4Cl可作化肥中的_________肥, 该厂的另一种产品碳酸氢钠俗称__________,它的重要用途有___________(只写一种)。
②实验室进行“过滤”操作时,下列说法正确的有_______(填字母)
A使用的漏斗叫长颈漏斗 B液面应低于滤纸边缘
C玻璃棒应不停搅拌 D漏斗下端的管口要紧靠烧杯内壁
(4)某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案:
方案一:称取样品10.65g,加水完全溶解,向其中加入足量的氯化钡溶液,充分反应后,过滤、洗涤,干燥得固体19.70g。通过计算(写出计算过程)判断该厂的产品是否属于优等品_________。(杂质可溶于水且不与氯化钡反应)
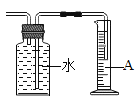
方案二:用如图所示的装置收集,通过准确测量排出水的体积,也可计算样品的纯度。该装置中仪器A的名称是___________,但实验后同学们发现所测的碳酸钠的纯度偏低,造成此结果的原因可能是_______。(装置的气密性良好)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了证明酸碱之间能够发生中和反应某同学设计了下列实验,请你回答有关问题:
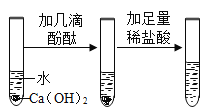
(1)氢氧化钙在农业上常用来改良________________(选填“酸性”或“碱性”)土壤;
(2)写出加入足量稀盐酸后试管内发生反应的化学方程式_____________;
(3)该实验达到了实验目的,最终你都能观察到明显现象有___________;
(4)该实验设计的原理是通过验证_________来设计的。
A 某种反应物的缺失 B 有新物质的生成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组发现,原本银白色有金属光泽的镁,漏置在空气中一段时间后,表面覆盖一层灰黑色物质。该小组同学进行了如下探究。
探究一:灰黑色物质成分
(猜想与假设)
小明说:灰黑色可能含有MgO、Mg(OH)2、Mg2(OH)2CO3。小芳说:不可能是MgO,原因是______________________________。
(进行试验)
实验编号 | 实验操作 | 实验现象 |
① | 取灰黑色粉末于试管中,滴加稀盐酸 | 有气泡产生 |
② | 将产生的气体通入澄清的石灰水中 | 石灰水变混浊 |
(得出结论)
得出结论灰黑色物质中一定含有________________;写出实验②中发生的化学方程式________________。
探究二:产生灰黑色物质的原因
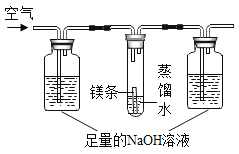
在猜想产生灰黑色物质的原因时,小华认为,镁条变黑与N2无关,其理由是____________。为进一步探究产生灰黑色物质的原因,设计如图实验,其中NaOH溶液的作用是_________________,经过一段时间,试管中镁条基本无变化。
(得出结论)镁表面的黑色物质是美与空气中O2、CO2、H2O共同作用的结果。
(实验拓展)①用镁条实验前一般要进行的操作是_______________。 ②保存镁条的方法是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对“真空充气包装食品”的探究。
背景1:市场上销售的豆腐干、盐水鸭等食品,常采用真空包装。真空包装的目的是:除去空气,使大多数微生物因缺少 而受到抑制,停止繁殖,从而防止食品变质。
背景2:“可比克”等膨化食品、蛋黄派等常采用真空充气包装,即将食品装入包装袋,抽出包装袋内的空气,再充入防止食品变质的气体,然后封口。真空充气包装能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形。
【提出问题】充入食品包装袋中的气体是什么?
【猜想假设】经过同学们的激烈讨论,最后同学们提出了气体可能的情况:
①氮气;②二氧化碳。
【提出方案】为了探究气体的成分,小华和小红两位同学各提出了一种方案。
①小华方案:收集一瓶该气体,把一根燃着的木条伸入瓶中,发现木条熄灭。由此得出气体是二氧化碳。该方案 可行(填“是”或“否”)?理由是 。
②小红的方案被同学们认可。走进食品生产工厂,在装有该气体的容器(容器内压强接近大气压强)上连接了如图一个装置。
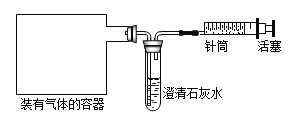
A、为了使容器内的气体通过澄清石灰水,活塞应向 (左或右)移动。
B、不管气体是二氧化碳还是氮气,试管中都有的实验现象是 。
C、经过实验后,发现澄清石灰水 ,证明气体是二氧化碳。
请写出该反应的表达式 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组物质鉴别方案的描述,正确的是( )
A.![]() 四种气体,用燃着的木条就能将其鉴别出来
四种气体,用燃着的木条就能将其鉴别出来
B.![]() 四种固体,只用水就能将其鉴别出来
四种固体,只用水就能将其鉴别出来
C.![]() 四种溶液,只用酚酞溶液及相互反应不能将其鉴别出来
四种溶液,只用酚酞溶液及相互反应不能将其鉴别出来
D.浓氨水、浓盐酸、稀硫酸、食盐水四种溶液,通过闻气味就能将其鉴别出来
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,是社会经济发展不可缺少和不可替代的重要自然资源和环境要素。
(1)2018年3月22日是第二十四届“世界水日”。为响应这一主题,某中学环保小组的同学配合环保部门,定期对我市大明湖的水进行取样测试。请根据某日采集的水样,回答以下问题:
①小黄同学取了少量大明湖水样品,观察到湖水并非无色透明,他可以加入适量________,用来除去水样中的异味和色素。
②为了保护大明湖的水质,下列做法不合理的是_________(填序号)。
A全面抑制湖中的植物生长 B不向湖水排放工业废水
C禁止游人向湖中乱扔垃圾 D定期对湖水水质进行监测
③环保小组的同学欲用pH试纸粗略测定大明湖水质的酸碱性强弱,请写出具体的操作方法:___________。
(2)如图所示为水的天然循环的一部分。
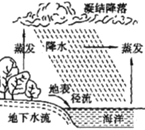
①海水属于_____(填“纯净物”或“混合物”)
②下列方法能从海水中获取淡水资源的是__________。
A过滤 B蒸馏 C沉降 D蒸发
(2)水和溶液对于人类的生产和生命活动有重大的意义。
①生活中,可以用________区分硬水和软水,通过______的方法将硬水软化。
②若用氯化钠固体和水配制0.9%的生理盐水,如图所示为相关的实验操作步骤:
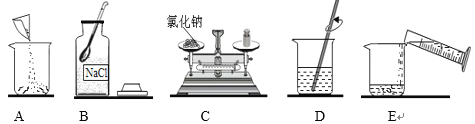
配制0.9%生理盐水的正确操作顺序是_______(填字母序号)。若用量筒量取水时仰视读数,其它操作均正确,则所配生理盐水的溶质质量分数_______0.9% 。(填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com