
【题目】我国民间有端午节吃粽子的习俗.“返青粽叶”是不法商贩用硫酸铜浸泡过的,误食这样的粽叶包的粽子有害健康.在物质分类中,硫酸铜属于
A.混合物 B.氧化物 C.盐 D.酸
科目:初中化学 来源: 题型:
【题目】在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题:

(1)该反应的文字表达式是 .
(2)小涵用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其操作上的原因可能是(要求答出两种):
① ;② .
(3)该实验还能证实剩余气体的性质(写出两点) , .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知NaHCO3在270℃时完全分解为碳酸钠、水和二氧化碳,而Na2CO3受热不分解.现有某工厂生产出的一批NaHCO3产品中混有少量的Na2CO3,某兴趣小组同学为了测定该产品中NaHCO3的质量分数,设计了下列两种实验方案.
方案一:样品![]() 测定生成CO2的质量.
测定生成CO2的质量.

(1)本实验采用如图所示的装置,C中盛放的物质是 .
(2)若把分液漏斗中的稀硫酸改为稀盐酸,在其他操作正确的情况下, (填“能”或“不能”)准确测定样品中NaHCO3的质量分数.
方案二:样品![]() 测定剩余固体质量.
测定剩余固体质量.
具体操作步骤如下:
①一只洁净的坩埚,称得质量为21.2克,再向其中加入样品,称得总质量为41.2克;
②加热盛有样品的坩埚;
③将坩埚充分冷却,称量坩埚和剩余固体的质量;
④多次重复步骤②和③至恒重,称得坩埚和剩余固体的总质量为35.0克.
(3)实验时需要重复“加热、冷却、称量”操作多次,其目的是 .
(4)根据题意,计算样品中NaHCO3的质量分数,写出计算过程.
(已知2NaHCO3![]() Na2CO3+H2O+CO2↑)
Na2CO3+H2O+CO2↑)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铈是一种常见的稀土元素,它在周期表中的相关信息如图所示.下列说法错误的是

A.铈原子的核外电子数为58
B.铈属于非金属元素
C.铈元素的元素符号是Ce
D.铈的相对原子质量是140.1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2015年9月29日定为扬州建城2500周年的城庆日。扬州因运河而生、因运河而兴,运河是扬州的母亲河。水是生命之源,面对严峻的缺水问题,我们要积极行动起来,合理利用和保护水资源,下列有关解决水资源危机的方法中,不可取的是
A.开发节水技术 B.防治水污染
C.植树造林,保护植被 D.大力开发地下水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是初中化学中的一些重要实验,请回答:
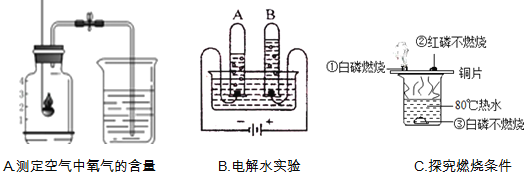
(1)A实验可知氧气约占空气总体积的 .
(2)B中与负极相连试管产生的气体是 .
(3)C中现象①②说明物质燃烧需要 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,有三种不同的实验装置,集气瓶中均充满空气,燃烧匙内所盛有的物质 (装置一中物质为红磷:装置二中物质为木炭;装置三中分别装有红磷和木炭)均为过量,大烧杯内盛有水.当充分燃烧后,冷却至室温,打开弹簧夹:

打开止水夹,请依次描述打开止水夹后三种装置所出现的现象及其原因:
(1)装置一中所出现的现象为 ,原因是 ;
(2)装置二中所出现的现象为 ,原因是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属是一类重要的材料,研究其性质十分必要.
(1)地壳中含量最多的金属元素是 .
(2)人们对铝的利用比铜和铁晚.金属大规模开发和利用的先后顺序与 (填序号)有关.
A.金属的活动性 B.金属的导电性 C.金属的导热性
(3)下面是某小组同学对金属镁和铁性质的对比研究.
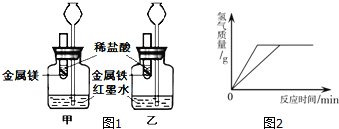
①在室温条件下进行图1所示实验.试管内的镁和铁表面均被打磨,且形状、大小均相同,向两支试管中同时加入相同的稀盐酸.通过观察到 现象,可得出的结论是金属活动性 > (填元素符号);还可以观察到反应在相同时间内,两支长颈漏斗的液面高度不同,可得出的结论是 .
②取等质量的镁、铁两种金属.将镁放入稀硫酸中,铁放入稀盐酸中,产生氢气的质量随反应时间变化曲线如图2下列说法正确的是 (填序号).
A.消耗铁的质量一定小于镁的质量
B.充分反应后,镁、铁一定都有剩余
C.充分反应后,溶液的质量一定都有所增加
D.充分反应后,稀硫酸和稀盐酸一定都没有剩余.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢
氧化钠溶液40g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4质量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com