
【题目】“碳汇”是指从空气中清除和吸收二氧化碳的过程与机制。科学家设想出碳捕捉技术,利用如下图所示的太阳能加热器完成CO2的“捕捉”和“释放”,实现碳循环。则回答:
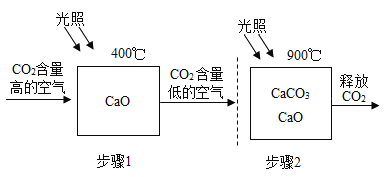
(1)碳捕捉的步骤1的化学方程式为___。步骤2中分离出的CO2可制成干冰,则干冰常用于____;
(2)上述中可循环利用的物质俗名为____,请说明这种碳捕捉设想的优点有哪些(至少一点)____。
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:初中化学 来源: 题型:
【题目】牙膏中常用碳酸钙、二氧化硅等物质作为摩擦剂。某同学对牙膏中摩擦剂碳酸钙的含量进行探究。
(实验原理)测定C装置中生成的BaCO 3 沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
(查阅资料)CO2+Ba(OH)2=BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生。
(实验装置)
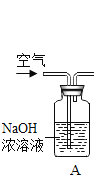
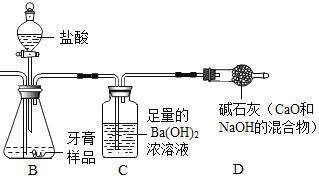
根据探究过程回答下列问题:
(1)装置A中氢氧化钠溶液的作用是_____。若没有A装置,直接通入空气,则测得CaCO3的质量分数_____(填“偏大”、“偏小”或“不变”)。装置B中发生反应的化学方程式为_____。
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C 中的反应物,使其充分反应;②_____。
(3)从C中过滤出BaCO3沉淀,所需的玻璃仪器有烧杯、_____和玻璃棒。
(4)只要测定装置C在吸收CO2前后的质量差,同样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,分析的原因是_______。
(5)为提高测定准确度,应采取必要措施,其中能达到目的的是____(填序号)。
①在加入盐酸之前,排净装置内的CO2气体
②放慢滴加盐酸的速度
③在A~B之间增添盛有浓硫酸的洗气装置
④在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取三份牙膏样品,每份4.0g,进行三次测定,测得生成BaCO3的平均质量为1.97g。则样品中CaCO3的质量分数为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E是初中化学常见的五种物质,其中A是钠盐,且A、D都由三种元素组成,E是红棕色固体,且与B在一定条件下反应有黑色粉末生成,C的固体可用于人工降雨。图中“—”表示两端物质间能发生反应,“→”表示物质间的转化关系,部分反应物、生成物及反应条件已略去。请回答下列问题:
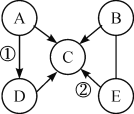
(1)写出下列物质的化学式:D_____________、C____________。
(2)写出反应①的化学方程:_______________,反应①属于__________________反应(填基本反应类型),
(3)B物质与E物质反应过程中,B物质具有______________(填“氧化性”或“还原性”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学反应的微观过程如图,则下列说法中,不合理的是( )
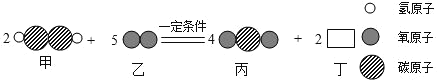
A.该反应属于置换反应B.生成物丙和丁均为氧化物
C.物质丁的化学式是H2OD.反应前后原子的种类、数目没有改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】稀土元素在科技生产中有广泛的用途,被誉为神奇的新材料宝库。如图分别是稀土大家族中镧、钇元素在元素周期表中的相关信息,下列说法不正确的是( )


A.镧与钇两种元素的本质区别在于质子数不同
B.稀土系储氢镧镍合金属于混合物
C.镧镍合金的熔点比镧、镍的熔点要高
D.钇的相对原子质量为88.91
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明将未打磨的铝片和稀盐酸放入密闭容器中,用传感器探究反应过程中温度和压强的变化,如右图所示。从图中所获信息不正确的是


A. 反应过程中有热量放出B. 50s时,溶液中溶质为AlCl3
C. 0~50s,发生Al2O3+6HCl===2AlCl3+3H2O反应D. 100—140s,压强减小是因为温度降低
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钠(Na2O2)是淡黄色固体,保存不当会变质而发白色。化学兴趣小组查得以下资料,对于过氧化钠变质的原理,有两种不同的原因:
甲:2Na2O2 + 2CO2 = 2Na2CO3 + O2
乙:2Na2O2 + 2H2O = 4NaOH + O2 ↑
为探究过氧化钠变质原理的合理性,开展以下实验。
(实验过程)
[实验1]取适量保存不当而变质发白色的固体于试管中,加入足量稀硫酸,产生无色无味的气 体,通入澄清石灰水中,澄清石灰水变浑浊。
(1)产生无色无味气体的原因_____(用化学方程式表示)。
(2)化学兴趣小组认为:据此现象,还不能得出“反应甲是造成过氧化钠变质的原因”的结论。理由是_____。
[实验 2]兴趣小组设计了如图 1 的实验装置,探究二氧化碳与过氧化钠反应。B 中盛有饱和碳酸氢钠溶液,C 中盛有浓硫酸。
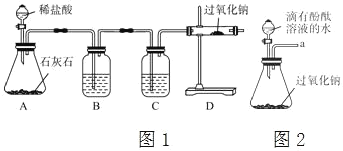
(3)B 中盛有饱和碳酸氢钠溶液,其作用是_____;C 中盛有浓硫酸,其作用是_____。
(4)在 D 中观察到_____现象时,说明二氧化碳与过氧化钠发生了化学反应。
[实验 3]兴趣小组按图 2 所示装置探究水和过氧化钠反应。
(5)检验有氧气生成的方法是_____。
(6)根据酚酞溶液变红色,可以检验有_____生成,实验过程中观察到溶液变红,后红色褪去。(老师提示:过氧化钠与水反应生成了一种不很稳定、具有漂白性的H2O2使酚酞由红色褪为无色。)
[实验4]水和过氧化钠反应产物的再探究
(7)另取水与过氧化钠反应后的无色溶液于烧杯中,加入二氧化锰,目的是_____,充分搅拌后,再滴加无色酚酞溶液,溶液变成红色且放置一段时间都不褪色。由此得出反应乙也是过氧化钠变质的原因。
(反思提高)
(8)过氧化钠与二氧化碳和水都会发生化学反应而变质,最终都生成碳酸钠,因此过氧化钠必须_____保存。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国最大钾盐产品基地出品多种含钾化合物。氯化钾可配制运动饮料,用于补充人体的电解质,最大允许使用氯化钾的质量分数为0.02%(水的密度为1g/cm3)。
(1)配制500g该种运动饮料,所需氯化钾的质量最多为__g;用托盘天平称量,氯化钾固体应放在_____(填“左盘”或“右盘”)。
(2)用量筒来量取所需的水,量筒的规格是_____(选用“50 mL”、“100 mL”或“500 mL”)。量取液体时,量筒必须放平,视线与液体的__________保持水平。
(3)若称取的氯化钾中含有水分,则所配制运动饮料的溶质质量分数会_______(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】京沪高铁将于2011年7月1日正式开通运营,采用了世界最先进中国铁路Ⅱ型板式轨道系统,该轨道系统以混凝土道板、底座结构代替传统铁路道砟,可以减小高速运行下列车振动噪声小,而且轨道几何平顺性好,乘客舒适度好。则回答:
(1)在高速铁路建设中使用大量材料:①铺路基的石子;②垫在石子上的钢筋水泥柱;③钢轨等,其中水泥柱属于(_____)
A金属材料B无机非金属材料C合成材料D复合材料
(2)为适应火车提速,高速铁路的短轨已全部连接为超长轨。施工建设中,常用点燃铝和氧化铁(Fe2O3)的混合物,反应时放出大量的热进行焊接铁轨中的缝隙,并生成氧化铝和熔融状态下的铁,从而焊接钢轨间的缝隙。则有关反应的化学方程式为___________,反应类型为______________,该反应过程中______能转化为热能,并说明铝的活动性比铁____(填“强”或“弱”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com