
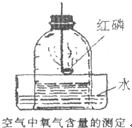
 某同学用如图装置(倒扣钟罩)来测定空气中氧气的含量.对该实验认识不正确的是( )
某同学用如图装置(倒扣钟罩)来测定空气中氧气的含量.对该实验认识不正确的是( )

 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:初中化学 来源: 题型:阅读理解
| 加热 |
| 加热 |
| 二氧化锰 |
| 二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:
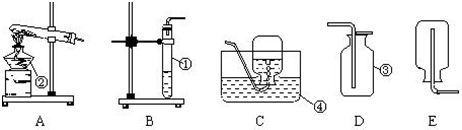
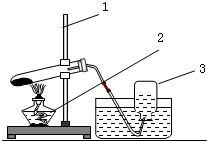 某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,回答问题:
某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:
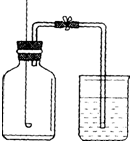
 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.| 实验操作 | 预期现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?北京二模)化学小组同学用如图所示装置(夹持仪器已略去)做兴趣实验.
(2013?北京二模)化学小组同学用如图所示装置(夹持仪器已略去)做兴趣实验.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.
某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.| 点燃 |
| 点燃 |
| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com