
 ≈33.3%.
≈33.3%.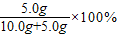 ≈33.3%;100g原溶液中溶质KCl的质量分数=
≈33.3%;100g原溶液中溶质KCl的质量分数= ×100%=25%≠33.3%;故A不正确;
×100%=25%≠33.3%;故A不正确; =50.0g;故B正确;
=50.0g;故B正确; ×100%=25%≠50%;故C不正确;
×100%=25%≠50%;故C不正确; ,即饱和溶液的溶质质量分数与溶液多少无关,其溶质质量分数都相等.
,即饱和溶液的溶质质量分数与溶液多少无关,其溶质质量分数都相等. 

科目:初中化学 来源: 题型:
 (2012?湖州)t℃时,两个装有100克水的烧杯中,分别加入不带结晶水的甲、乙物质各80克,充分搅拌.根据如图溶解度曲线判断,此时
(2012?湖州)t℃时,两个装有100克水的烧杯中,分别加入不带结晶水的甲、乙物质各80克,充分搅拌.根据如图溶解度曲线判断,此时查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:自贡 题型:问答题

查看答案和解析>>
科目:初中化学 来源:2013年四川省自贡市中考化学试卷(解析版) 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:
t1 ℃ 时,分别将20g甲、乙两种晶体(不含结晶水)加入盛有100g水的两个烧杯中,恰好完全溶解,升温到t时出现甲、乙烧杯中所示的现象。根据上述实验,结合下图中甲、乙两 物质的溶解度曲线,判断下列说法正确的是

A t1℃时烧杯中甲、乙两物质形成的溶液是不饱和溶液
B t1℃时烧杯中甲、乙两物质形成的溶液溶质质量分数约为16 7%
C. t2℃时烧杯中甲物质溶液的质量是110g
D. t2℃时乙物质的溶解度是130g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com