
分析 根据高锰酸钾受热分解后生成锰酸钾、二氧化锰和氧气,由于氧气逸出,所以反应后固体质量会减少;根据质量守恒定律可知,固体质量的减少量即为生成氧气的质量,然后根据反应的化学方程式由氧气的质量求出参加反应的高锰酸钾及生成的锰酸钾和二氧化锰的质量进行分析.
解答 解:(1)制得氧气的质量为:15.8g-15g=0.8g;
(2)设参加反应的KMnO4质量为x,生成的K2MnO4质量为y,生成MnO2质量为z.
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4 +MnO2 +O2↑
316 197 87 32
x y z 0.8g
$\frac{316}{x}$=$\frac{197}{y}$=$\frac{87}{z}$=$\frac{32}{0.8g}$
x=7.9g
y=4.925g
z=2.175g
15克的剩余物质中高锰酸钾、锰酸钾和二氧化锰,其质量分别是:15.8g-7.9=7.9g、4.925g、2.175g.
故答案为:(1)0.8g;
(2)高锰酸钾、锰酸钾和二氧化锰,其质量分别是:7.9g、4.925g、2.175g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气气的质量是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:计算题
| 浓硫酸(H2SO4)500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
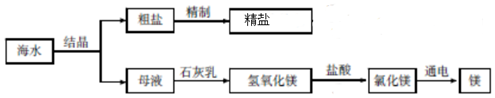
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石墨含量越高铅笔芯的导电性越好 | |
| B. | 只有电解水的实验才能确定水的组成 | |
| C. | 加热含氧化合物都能得到氧气 | |
| D. | 用放大镜观察蔗糖,可看到蔗糖分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  验证白磷的着火点比红磷低 | |
| B. |  验证二氧化碳能与氢氧化钠溶液反应 | |
| C. | 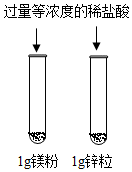 比较镁、锌的活动性顺序 | |
| D. | 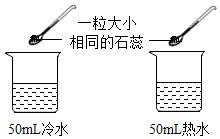 探究温度对分子运动的影响 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 16 g | B. | 21 g | C. | 24 g | D. | 32 g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯酸钾 | B. | 氧气 | C. | 水 | D. | 氧元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com