
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| 将NaOH溶液加热煮沸 | 煮沸能达到此目的理由是除去氢氧化钠溶液中溶解的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想 正确 (填“正确”或“不正确”) |
| 向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | 隔绝氧气 |
分析 【设计实验】
(1)根据氢氧化钠溶液呈碱性,能使酚酞试液变红,氢氧化钠与空气中的二氧化碳反应生成的碳酸钠水溶液呈碱性,也能使酚酞试液变红解答;
(2)甲同学认为“可能是酚酞与O2发生了反应”,隔绝氧气,设计了实验;
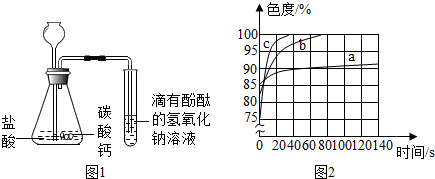
(3)乙同学认为“可能是NaOH溶液与空气中的CO2发生了反应”,设计如图1装置进行实验,则正确写出CO2与NaOH溶液反应的化学方程式,考虑二氧化碳中可能混有氯化氢气体;
(4)认真分析题图可以得出:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越大,起始颜色越深.从图中看5%的NaOH溶液滴加2滴酚酞试液后140s内色度从85升高至92,那么从92升高至100,所需时间要大于140s.
解答 解:【设计实验】
(1)氢氧化钠与二氧化碳反应生成的碳酸钠溶液呈碱性,能使酚酞变红,所以本题答案为:氢氧化钠溶液与空气中的二氧化碳反应生成碳酸钠和水,碳酸钠水溶液显碱性;开始时酚酞变红,若是酚酞变质,则开始时不会变成红色,所以本题答案为:若酚酞变质,刚开始溶液就不会变红色;
(2)甲同学设计了如下实验验证自己的猜想:
将NaOH溶液加热煮沸,煮沸能达到此目的理由是除去氢氧化钠溶液中溶解的氧气,向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方,目的是隔绝氧气;溶液变红,过一会儿红色消失,甲同学猜想正确;
(3)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.一段时间后,试管中溶液的红色褪去,则正确写出CO2与NaOH溶液反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O;考虑二氧化碳中可能混有氯化氢气体,因为若制取的二氧化碳气体中混有氯化氢气体,则氢氧化钠与氯化氢发生反应,则试管中溶液的红色也能褪去;
(4)认真分析题中图可以得出:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越大,起始颜色越深.从图中看5%的NaOH溶液滴加2滴酚酞试液后140s内色度从85升高至92,那么从92升高至100,所需时间要大于140s.
答案:
(1)氢氧化钠溶液与空气中的二氧化碳反应生成碳酸钠和水,碳酸钠水溶液显碱性;若酚酞变质,刚开始溶液就不会变红色;
(2)
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| 将NaOH溶液加热煮沸 | 煮沸能达到此目的理由是 除去氢氧化钠溶液中溶解的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想 正确 (填“正确”或“不正确”) |
| 向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | 隔绝氧气 |
点评 本题考查了酚酞的变色与氢氧化钠浓度的关系,完成此题,可以依据已有的知识进行,设计实验时要注意实验变量的控制.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:初中化学 来源: 题型:解答题
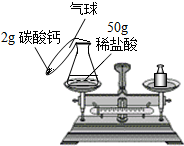 小明同学欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸钙反应”为研究对象,设计的实验装罝如图所示.
小明同学欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸钙反应”为研究对象,设计的实验装罝如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
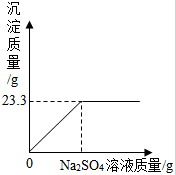 称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的查看答案和解析>>
科目:初中化学 来源: 题型:填空题

 表示的是(写粒子符号)Ca2+.
表示的是(写粒子符号)Ca2+.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe2O3+4HCl═2FeCl2+2H2O | B. | Al(OH)3+3HCl═AlCl3+3H2O | ||
| C. | Cu+H2SO4═H2↑+CuSO4 | D. | KNO3+NaCl═KCl↓+NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁带在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 | |
| B. | 在点燃的条件下,磷在氧气中剧烈燃烧,产生大量白雾 | |
| C. | 在点燃的条件下,硫在氧气里燃烧,发出蓝紫色火焰,生成无色无味的气体 | |
| D. | 在点燃的条件下,细铁丝在氧气中剧烈燃烧,火星四射,生成黑色的三氧化二铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com