
分析 (1)根据甲烷燃烧生成二氧化碳和水写出反应的化学方程式即可.
(2)根据反应的原理以及化学方程式的写法分析解答.
(3)根据一氧化碳有毒分析解答.
解答 解:(1)甲烷燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)24g甲烷和80g氧气燃烧生成54g水、22gCO2的同时,生成一氧化碳的质量为24g+80g-54g-22g=28g;化学方程式中,甲烷、氧气、水、二氧化碳、一氧化碳的化学式前面化学计量数之比为 $\frac{24g}{16}$:$\frac{80g}{32}$:$\frac{54g}{18}$:$\frac{22g}{44}$:$\frac{28g}{28}$=3:5:6:1:2,因此化学方程式为:3CH4+5O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+CO2+2CO.
(3)在密闭的卫生间内氧气不充足,天然气不充分燃烧生成了一氧化碳,一氧化碳有毒,易造成煤气中毒.
故答案为:(1)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;(2)3CH4+5O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+CO2+2CO;(3)密闭卫生间内氧气不充足,天然气不充分燃烧生成一氧化碳,可能导致煤气中毒.
点评 在解此类方程式的书写题时,首先根据反应找出反应物、生成物和反应条件,再根据方程式的书写规则书写方程式.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中燃烧时火星四射,有四氧化三铁生成 | |
| B. | 打开浓盐酸试剂瓶的瓶塞,瓶口上方出现大量白烟 | |
| C. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| D. | 铁锈与稀盐酸反应后溶液由无色变成了浅绿色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用白酒区分食盐和纯碱 | |
| B. | 用灼烧的方法区分羊毛制品和涤纶制品. | |
| C. | 用加铁酱油与食醋反应制氢气 | |
| D. | 用汽油洗掉白衬衫上的铁锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 元素周期表是学习化学的重要依据.如图是元素周期表的一部分,四位同学按表格提供的信息进行判断,其中判断错误的是( )
元素周期表是学习化学的重要依据.如图是元素周期表的一部分,四位同学按表格提供的信息进行判断,其中判断错误的是( )| A. | 小春说:碳、氢、氧三种元素都属于非金属元素 | |
| B. | 小夏说:不同种元素之间最本质的区别是最外层电子数不同 | |
| C. | 小秋说:氧原子的核内中子数是8 | |
| D. | 小冬说:氮原子的相对原子质量是14.01 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
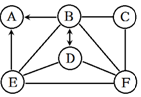 A、B、C、D、E、F是初中常见的物质,其中A可参与光合作用,B是酸溶液,C为黑色粉末,D为钡盐溶液,E溶液显碱性,F为盐溶液,它们之间的转化关系如图所示(“→”表示一种物质可以转化另一种物质,“--”表示两种物质间能发生反应,图中已略去部分物质),
A、B、C、D、E、F是初中常见的物质,其中A可参与光合作用,B是酸溶液,C为黑色粉末,D为钡盐溶液,E溶液显碱性,F为盐溶液,它们之间的转化关系如图所示(“→”表示一种物质可以转化另一种物质,“--”表示两种物质间能发生反应,图中已略去部分物质),查看答案和解析>>
科目:初中化学 来源: 题型:计算题
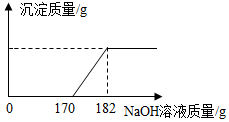 工业盐酸中常混有少量的FeCl3而呈黄色.为测定某工业盐酸中FeCl3的含量进行如下实验:取该工业盐酸100g,滴加溶质质量分数为20%的NaOH溶液,加入NaOH溶液质量与反应生成的沉淀质量关系如图所示.FeCl3与NaOH反应的化学方程式为:FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
工业盐酸中常混有少量的FeCl3而呈黄色.为测定某工业盐酸中FeCl3的含量进行如下实验:取该工业盐酸100g,滴加溶质质量分数为20%的NaOH溶液,加入NaOH溶液质量与反应生成的沉淀质量关系如图所示.FeCl3与NaOH反应的化学方程式为:FeCl3+3NaOH═Fe(OH)3↓+3NaCl.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com