
【题目】依据溶解度知识回答下列小题。
下表为NaOH、Na2CO3、NaCl、Ca(OH) 2分别在水中的溶解度(g)
t/°C | NaOH | Na2CO3 | NaCl | Ca(OH)2 |
10 | 51 | 12. 2 | 35. 8 | 0. 17 |
10℃时,向4只盛有100 g水的烧杯中分别加入40 g上述四种物质配成溶液,依据上表回答下列小题。
【1】上述溶液为不饱和溶液的是
A. Ca(OH) 2 溶液B. Na2CO3 溶液C. NaCl 溶液D. NaOH 溶液
【2】上述溶液中,溶质质量分数最大的是
A. Na2CO3 溶液B. NaOH 溶液C. NaCl 溶液D. Ca(OH) 2 溶液
【3】关于上述形成的Na2CO3溶液,下列说法正确的是
A. 溶质的质量为40 g
B. 溶液的质量为140 g
C. 该烧杯底部有未溶解的固体
D. 10℃时,100 gNa2CO3溶液里含有12.2 g碳酸钠
【4】下图为氯化钠、碳酸钠在水中的溶解度曲线。依据图像判断,下列说法正确的是

A. 碳酸钠的溶解度小于氯化钠的溶解度
B. 20℃时,氯化钠溶液的质量分数一定小于碳酸钠溶液
C. 30℃时,两种物质的饱和溶液中溶质质量相等
D. 将Na2CO3和NaCl均达到饱和的混合溶液,从40℃降温至20℃时,析出的固体物质主要是Na2CO3
【答案】
【1】D
【2】B
【3】C
【4】D
【解析】
【1】A、10℃时,Ca(OH)2的溶解度为0.17g,则向100g水的烧杯中加入40gCa(OH)2没有完全溶解,该溶液是饱和溶液,故错误;
B、10℃时,Na2CO3的溶解度为12.2g,则向100g水的烧杯中加入40gNa2CO3没有完全溶解,该溶液是饱和溶液,故错误;
C、10℃时,NaCl的溶解度为35.8g,则向100g水的烧杯中加入40gNaCl没有完全溶解,该溶液是饱和溶液,故错误;
D、10℃时,NaOH的溶解度为51g,则向100g水的烧杯中加入51gNaOH才能达到饱和状态,该溶液是不饱和溶液,故正确;
故选:D。
【2】10℃时,四种物质的溶解度中NaOH的最大,所以溶质质量分数最大的是NaOH溶液,
故选:B。
【3】10℃时,Na2CO3的溶解度是12.2g,
A、溶质的质量为12.2g,故说法错误;
B、溶液的质量为:100g+12.2g=112.2g,故说法错误;
C、溶质的质量为12.2g,则有27.8g溶质没有溶解,则该烧杯底部有未溶解的固体,故说法正确;
D、10℃时,112.2gNa2CO3溶液里含有12.2g碳酸钠,故说法错误;
故选:C。
【4】A、碳酸钠的溶解度小于氯化钠的溶解度错误,因为没有指明温度;故选项错误;
B、20℃时,氯化钠溶液的质量分数一定小于碳酸钠溶液错误,因为没有指明溶液的状态;故选项错误;
C、30℃时,两种物质的饱和溶液中溶质质量相等错误,因为没有指明是等质量的饱和溶液;故选项错误;
D、将Na2CO3和NaCl均达到饱和的混合溶液,从40℃降温至20℃时,析出的固体物质主要是Na2CO3正确,因为碳酸钠的溶解度受温度的影响变化比氯化钠大;故选项正确;
故选:D。


科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
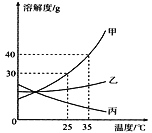
(1)25℃时,将20g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为____g。
(2)要使35℃时接近饱和的丙溶液变成该温度下的饱和溶液,可采用的一种方法是______。
(3)现有操作步骤:A.溶解B.过滤C.降温结晶D.加热浓缩。若甲固体中含有少量乙,则提纯甲的操作步骤的顺序是___________(填字母序号)。
(4)若将35℃时甲的饱和溶液降温到25℃,则其溶液的溶质质量分数会___。(填“变大”“变小”或“不变”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蜡烛(足量)在如图1密闭的集气瓶内燃烧至熄灭,用仪器测出瓶内氧气含量的变化如图2所示。下列判断正确的是
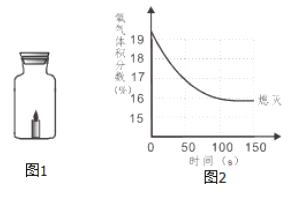
A. 蜡烛燃烧前瓶内只有氧气
B. 蜡烛熄灭是因为瓶内没有氧气
C. 蜡烛熄灭后瓶内只剩二氧化碳气体
D. 氧气浓度小于一定值时,蜡烛无法燃烧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
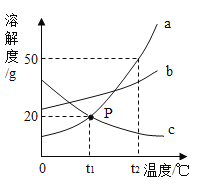
(1)P点的含义是______________________________________。
(2)t2 ℃时30ga物质加入到50 g水中不断搅拌,能形成溶液的质量_________.计算所得溶液的溶质质量分数_________。
(3)t2℃时a、b、c三种物质的溶解度按由大到小的顺序排列是_____________________(填写物质序号)。
(4)将t2℃时a、b、c三种物质饱和溶液的温度降低到t1℃时,三种溶液的溶质质量分数大小关系是______________(填写选项序号)。
A c>a=b B a=b>c C a>b>c D b>a>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁及其化合物在人类生产、生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是一种黑色的氧化物,它是_______。

A Fe B.FeO C Fe3O4 D Fe2O3
(2)卟啉铁[C34H32ClFeN4O4]是纯天然的生物补铁剂,常用于制作补铁口服液。人体适量补铁可预防__________。
(3)现代利用铁的氧化物循环裂解水制取氢气的过程如下图所示。
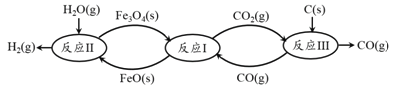
回答下列问题:
①该生产过程中产生氢气的化学方程式为__________。
②该反应过程中化合价发生改变的元素有___________________种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】联合钢铁工业的基本生产流程示意图如下:
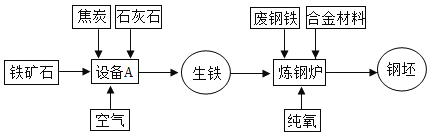
请回答下列问题:
(1) 焦炭的主要成分是(填名称或化学式)______。
(2) 写出用一氧化碳还原赤铁矿(Fe2O3)制取铁的化学方程式______。
(3) 现有含Fe2O3 160 t的赤铁矿,计算理论上可冶炼出纯铁的质量是______t。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图所示实验验证质量守恒定律。

(1)甲同学设计的实验如图A所示,将铁钉浸到硫酸铜溶液中,当观察到______时,进行第二次称量,指针位置保持不变。
(2) 乙同学设计的实验如图B所示,反应后托盘天平的指针______ (选填“向左”、“向右”或“不”)偏转。
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在______装置中进行。
(4) 从微观角度分析质量守恒的原因是______ (填序号)。
A 原子种类不变 B 分子种类不变
C 原子质量、数目不变 D 分子质量、数目不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】低碳生活能减少能源消耗,从而节约资源、减少CO2的排放。
(1)下列做法不属于低碳生活的是_________(填字母)。
A.使用节能灯 B.双面使用打印纸 C.多用塑料袋
(2)自然界“消耗CO2”的主要途径是___________________________。
(3)从火力发电厂的尾气中捕捉的CO2纯度很高,可制成固态做食品保鲜剂,固态二氧化碳俗称_________;CO2还可以被封存在地下咸水层,最终转化为固态碳酸盐。
(4)甲醇可添加到汽油中制成甲醇汽油。在催化剂的作用下,CO2与H2反应生成甲醇(CH4O)和H2O,该反应化学方程式为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示粒子的结构示意图回答问题:
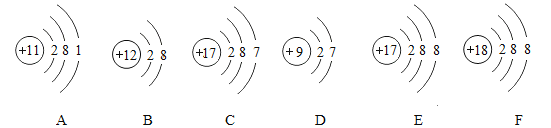
(1)具有相对稳定结构的微粒是_______(填序号,下同)
(2)在化学反应中易得到电子的微粒是 ______;
(3)表示阳离子的微粒是________;
(4)化学性质相似的原子是 __________
(5)A和C具有相同的是________(填序号)。
①质子数 ②电子数 ③电子层数 ④最外层电子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com