
 ¾ŻŠĀĪÅ”¶Ņ»³”Óź£¬Č“ŌŚŅ»Ęš»šŌÖµ±ÖŠ³äµ±ĮĖ”°ÓĶ”±µÄ½ĒÉ«”·±ØµĄ£ŗ30Ć×¹Ņ³µŅ»Ā·Čö”°»šÖÖ£¬½ÄĻ“󵥔°µē¹ā»šŹÆ”±13Š”Ź±£”ÕāŅ»ĒŠ¶¼ŹĒŅņĪŖŅ»Į¾ŌŲÓŠ20¶ą¶ÖµēŹÆµÄ“ó»õ³µ£®
¾ŻŠĀĪÅ”¶Ņ»³”Óź£¬Č“ŌŚŅ»Ęš»šŌÖµ±ÖŠ³äµ±ĮĖ”°ÓĶ”±µÄ½ĒÉ«”·±ØµĄ£ŗ30Ć×¹Ņ³µŅ»Ā·Čö”°»šÖÖ£¬½ÄĻ“󵥔°µē¹ā»šŹÆ”±13Š”Ź±£”ÕāŅ»ĒŠ¶¼ŹĒŅņĪŖŅ»Į¾ŌŲÓŠ20¶ą¶ÖµēŹÆµÄ“ó»õ³µ£®·ÖĪö øł¾Ż·“Ó¦Īļ”¢Éś³ÉĪļ”¢·“Ó¦Ģõ¼ž¼°ĘäÖŹĮæŹŲŗć¶ØĀÉæÉŅŌŹéŠ“·“Ó¦µÄ»Æѧ·½³ĢŹ½£»
øł¾ŻĘųĢåµÄŠŌÖŹæÉŅŌŃ”ŌńŹż¾Ż×°ÖĆ£®
½ā“š ½ā£ŗ£Ø1£©Ģ¼»ÆøĘÓöĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCaC2+2H2O=C2H2”ü+Ca£ØOH£©2£»
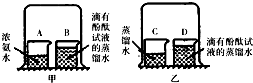
£Ø2£©ŅŅČ²ĘųĢå²»Ņ×ČÜÓŚĖ®£¬æÉŅŌÓĆÅÅĖ®·ØŹÕ¼Æ£¬¼“ÓĆA×°ÖĆŹÕ¼Æ£¬ĆܶȱČæÕĘųŠ”£¬æÉŅŌÓĆĻņĻĀÅÅæÕĘų·ØŹÕ¼Æ£¬¼“ÓĆC×°ÖĆŹÕ¼Æ£®
¹ŹĢī£ŗCaC2+2H2O=C2H2”ü+Ca£ØOH£©2£»A”¢C£®
µćĘĄ ŹéŠ“»Æѧ·½³ĢŹ½ŅŖ×¢ŅāĖIJ½£ŗŅ»ŹĒ·“Ó¦ĪļŗĶÉś³ÉĪļµÄ»ÆѧŹ½ŅŖÕżČ·£»¶žŹĒŅŖ×ńŃÖŹĮæŹŲŗć¶ØĀÉ£¬¼“ÅäĘ½£»ČżŹĒŅŖÓŠ±ŲŅŖµÄĢõ¼ž£»ĖÄŹĒæ“ŹĒ·ńŠčŅŖ”°”ü”±»ņ”°”ż”±£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĮņĖįŠæČÜŅŗ”¢ĢśŗĶĶŃéÖ¤Šæ”¢Ģś”¢ĶµÄ»ī¶ÆŠŌĖ³Šņ | |
| B£® | ÓĆĻą»„æĢ»µÄ·½·Ø±Č½Ļ»ĘĶŗĶĶµÄÓ²¶Č | |
| C£® | ÓĆÕŗĖ®ŗĶ¾Ę¾«µÄĮ½øöĆŽ»ØĶÅĢ½¾æČ¼ÉÕŠčŅŖæÉČ¼Īļ | |
| D£® | ÓĆŗģĮײā¶ØæÕĘųÖŠŃõĘųµÄŗ¬Įæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½ĢæĘŹéŃ»·Ź¹ÓĆ | B£® | QQ³¤Ź±¼ä¹Ņ»ś | C£® | ½ĢŹŅĪŽČĖŅŖ¹ŲµĘ | D£® | ³öŠŠ³Ė×ų¹«½»³µ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe+O2 $\frac{\underline{\;µćČ¼\;}}{\;}$Fe2O3 | B£® | H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$H2+O2 | ||
| C£® | 2Mg+O2$\frac{\underline{\;µćČ¼\;}}{\;}$2MgO | D£® | 2Fe+3 H2SO4Fe2£ØSO4 £©3+3 H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ„ÖŹ | B£® | Ō×Ó | C£® | Ąė×Ó | D£® | ŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com