
【题目】下列关于干冰升华过程的说法正确的是
A.二氧化碳分子的体积变大 B.二氧化碳分子的质量变小
C.二氧化碳分子的种类改变 D.二氧化碳分子间的间隔变大
科目:初中化学 来源: 题型:
【题目】 “端午佳节,粽叶飘香”,我们过节有吃盐蛋、粽子、糖包、肉包的习俗,从均衡营养的角度分析,还需要补充的主要营养素是( )
A.蛋白质 B.糖类 C.维生素 D.油脂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学方法改造物质——“二氧化碳变汽油”二氧化碳是化石燃料燃烧的产物,汽油(主要成分为含有5个-11个碳原子的碳氢化合物)是全球用量晟大的液体燃料。如果有人告诉你“二氧化碳能变成汽油”,你相信吗?
近日,中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过图2示意的I、II、III三个环节,将二氧化碳成功转化为汽油。(图中a、b是两种起始反应物的分子结构模型,c、d是最终制得的汽油中所含物质的分子结构模型)
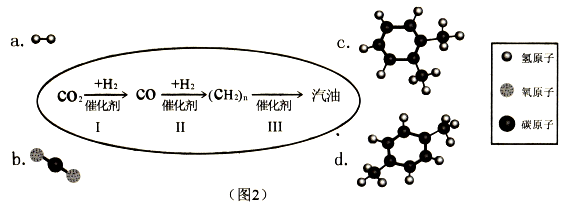
请回答下列问题:
(1)要实现物质间的转化,往往需要有高效的催化剂。下列有关催化剂的叙述正确的是____(填字母编号)。
A.催化剂可以改变化学反应速率
B.化学反应前后催化剂的质量不变
C.化学反应前后催化剂的化学性质发生改变
(2)在一定温度、一定压强和催化剂存在的条件下,环节I除生成CO外,还生成了一种化合韧,则反应的化学方程式为_____________。该反应中,二氧化碳中的部分氧元素被氢气夺去,二氧化碳发生了____反应。
(3)从物质类别的角度看,环节II实现了____的转化。
(4)认真观察c和d两种物质的分子结构模型,试写出c物质的分子式____,c和d的分子式是否相同?____,二者是否为相同物质?______,d物质中碳元素和氢元素的质量比为____。
(5)“二氧化碳变汽油”的研究成果,使我国成为此领域的世界领跑者。你认为该成果的现实意义是___________________,________________(答出两条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在托盘天平的两盘上各放一只质量相同的烧杯,分别加入等质量、等溶质质量分数的足量稀盐酸,将天平调节至平衡.然后向左盘的烧杯中加入4.0含钙元素的质量分数为50%的碳酸钙与氧化钙的固体混合物,使之完全反应.欲使天平恢复平衡,可向右盘的烧杯中加入( )
A.3.5g氢氧化钠溶液 B.2.8g氧化铁 C.2.8g碳酸钠溶液 D.2.4g镁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】十三五期间,烟台将建设大型海水淡化厂.绿色生态、综合利用海洋资源将是设计的重点.如图是某设计院设计的综合利用海水的流程图.据图回答问题:
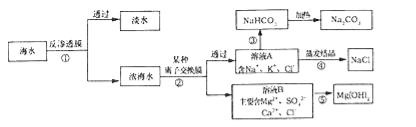
(1)反渗透膜法与滤纸过滤法在原理上都是利用混合体系中各物质的 不同进行分离的方法.
(2)过程③是氨碱法制纯碱的一个流程,需要向饱和食盐水中先后加入的两种物质是 (写化学式).
(3)过程④采用蒸发结晶的方法,而不采用冷却热饱和溶液方法,原因是 .
(4)如果要充分利用海边贝壳资源,过程⑤生成氢氧化镁的化学方程式是 .
(5)浓海水中Mg2+、SO42﹣、Ca2+,可用离子交换膜直接除去,若用化学沉淀法依次除去Mg2+、SO42﹣、Ca2+,需要的三种离子分别是 (写离子符号).
(6)离子交换膜是对特定离子的选择性透过膜,可以使带特定电量的离子透过.过程②中“某种离子交换膜”选择透过的离子特点是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验.
【实验一】(已知:白磷的着火点为40℃)
实验装置 | 实验步骤及现象 |
| 步骤Ⅰ.检验装置的气密性,气密性良好. 步骤Ⅱ.将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧. 步骤Ⅲ.向A瓶中加满80℃热水,塞紧瓶塞,白磷不燃烧. 步骤Ⅳ.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2.此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧. |
(1)对比步骤Ⅱ和Ⅳ的现象可知,可燃物燃烧的条件之一是
(2)待装置冷却一段时间后,打开K2,如果观察到 ,说明空气中氧气的体积约占![]() .若实验测得空气中氧气的体积分数小于
.若实验测得空气中氧气的体积分数小于![]() ,原因可能是 (答一条即可).
,原因可能是 (答一条即可).
【实验二】用如图所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量.若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由 .【已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿.化学方程式:2Cu+O2+H2O+CO2═Cu(OH)2CO3】
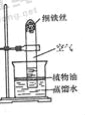
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年4月长春应用化学研究所提出了一种独特的锂-氮电池(Li-N2),结构示意图见下方。该电池由锂箔作负极,多孔碳布作正极,玻璃纤维作隔板,可以利用空气中的氮气,锂-氮电池反应方程式:6Li+N2=2Li3N。请回答:

(1)氮气在空气中的含量约为_____________________。
(2)Li3N中氮元素的化合价为________________________。
(3)锂原子的原子核内质子数为______________,它在化学反应中易_________(填“得到”或“失去”)电子。
(4)玻璃纤维是玻璃熔融状态下抽成丝制得,它属于_______(填序号)。
A.无机非金属材料 B.金属材料 C.有机高分子材料
(5)碳布作为锂-氮电池的电极,是利用了碳单质的_________(填一种物理性质即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某废液M可能含有硫酸钠、氯化钠、碳酸钠、氢氧化钠中的一种或几种,为确定其成分进行实验。

①反应生成气体的化学方程式是_______________。
②M中一定没有____________。
③为进一步确定M的成分,进行实验,步骤如下:
Ⅰ 重新取M样品,滴加过量的试剂X,静置;
Ⅱ 取Ⅰ中的上层清液,滴加酚酞;
Ⅲ 向Ⅱ中的溶液滴加过量的稀硝酸;
Ⅳ 向Ⅲ中的溶液滴加试剂Y。
完成填空:
试剂X是________(选填“氯化钡”或“硝酸钡”)溶液;试剂Y是________溶液。能确定M中含有氢氧化钠的最主要的一个现象是________;能确定M中含有氯化钠的最主要的一个现象是__________。(需写明现象对应的步骤编号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com