
 硫酸铵
硫酸铵 氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问
氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问 =
=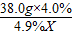
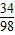 =
=
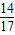 ×100%=0.168g
×100%=0.168g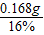 =1.05g
=1.05g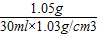 ×100%=3.4%
×100%=3.4%

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:初中化学 来源: 题型:
| ||
| 分解 |
| ||
| 水蒸气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
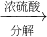 硫酸铵
硫酸铵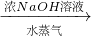 氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问
氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问查看答案和解析>>
科目:初中化学 来源:同步题 题型:计算题
 硫酸铵
硫酸铵 氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问
氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问查看答案和解析>>
科目:初中化学 来源:《第8章 食品中的有机化合物》2010年单元测试卷(8)(解析版) 题型:解答题
 硫酸铵
硫酸铵 氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问
氨,为了测定某牛奶样品中蛋白质的含量,取30mL牛奶用盖尔达法分离蛋白质,把氮元素完全转化成氨(NH3),用50g4.9%稀H2SO4溶液吸收后,剩余的酸需要用38.0g4.0%的NaOH溶液中和,问查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com