
分析 (1)物质的化学性质是指在化学变化中表现出来的性质.化学性质主要有:可燃性、毒性、氧化性、还原性、稳定性等.
物质的物理性质是指不需要通过化学变化表现出来的性质.物理性质主要有:颜色、状态、气味、密度、硬度、熔点、沸点等;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(3)根据化学反应前后碳元素质量守恒和化学式计算.
解答 解:(1)在16.6℃以上纯净的乙酸是一种有强烈刺激性气味的无色液体,易溶于水和酒精.这些描述属于醋酸的物理性质.
刺激性气味、无色液体、凝固点为16.6℃、易溶于水(任写一点即可);
(2)醋酸跟氢氧化钠溶液反应生成醋酸钠和水,反应的化学方程式为:CH3COOH+NaOH═CH3COONa+H2O;
(3)乙酸乙酯燃烧生成二氧化碳和水,所以乙酸乙酯中一定含有碳元素和氢元素,可能含有氧元素;二氧化碳中碳元素的质量分数为$\frac{12}{44}$,氧元素的质量分数为$\frac{16×2}{44}$=$\frac{32}{44}$;水中氢元素质量分数为$\frac{2}{18}$,氧元素质量分数为$\frac{16}{18}$;44g二氧化碳中碳元素的质量为:88g×$\frac{12}{44}$=24g,氧元素的质量为88g×$\frac{32}{44}$=64g;36g水中氧元素的质量为36g×$\frac{16}{18}$=32g,氢元素的质量为36g×$\frac{2}{18}$=4g;反应前后元素的质量不变,所以88g乙酸乙酯中碳元素的质量为24g,氢元素质量为4g,所以乙酸乙酯中碳元素和氢元素质量比是24:0.4=6:1,设乙酸乙酯的化学式为CxHyOz;乙酸乙酯中碳、氢元素质量比是12x:y=6:1,$\frac{x}{y}$=$\frac{1}{2}$;根据质量守恒定律参加反应的氧气质量为:88g+36g-44g=80g,44g乙酸乙酯中氧元素的质量44g-24g-4g=16g,乙酸乙酯中氢氧元素质量比是:4g:16g=1:4,$\frac{y}{16z}$=$\frac{1}{4}$,$\frac{y}{z}$=$\frac{4}{1}$
故答案:(1)刺激性气味、无色液体、凝固点为16.6℃、易溶于水;(2)CH3COOH+NaOH═CH3COONa+H2O(或HAc+NaOH═NaAc+H2O);(3)24克;(4)C4H8O2.
点评 本题主要考查了根据化学式的计算和根据化学方程式的计算,应用质量守恒思想上解答该题的关键,有一定的难度.


科目:初中化学 来源: 题型:选择题
| 选项 | 事实 | 解释 |
| A | 酒精温度计受热液柱上升 | 原子间间隔受热变大 |
| B | 碳酸钠溶液显碱性,稀硫酸显酸性 | 不同种物质的分子化学性质不同 |
| C | 氨水和氢氧化钠溶液都能使酚酞溶液变红 | 溶液中都含有相同的阴离子 |
| D | 金刚石和石墨的性质差异较大 | 碳原子的结构不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | m1=m2 | |
| B. | 25m1=21m2 | |
| C. | 混合物A中CaCO3和KHCO3质量比一定为1:1 | |
| D. | 混合物B中MgCO3和NaHCO3质量比可为任意比 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
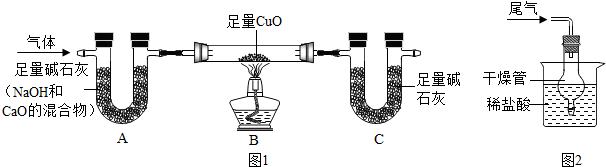
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
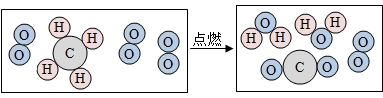
| A. | 该反应中甲烷分子和水分子的个数比是1:2 | |
| B. | 该反应的生成物有3种物质 | |
| C. | 该反应发生的条件是点燃,化学反应前后原子的种类和数目不变 | |
| D. | 该模型可说明:化学变化的实质是分子分成原子,原子重新组合成新分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | NaOH溶液 | NaCl | 加入适量稀盐酸 |
| B | NaCl溶液 | Na2SO4 | 加入适量硝酸钡溶液,过滤 |
| C | CaCl2溶液 | 稀盐酸 | 加入过量碳酸钙,过滤 |
| D | CO2 | CO | 通入O2,点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | a=b≥2.4g | B. | a=b≥1.8g | C. | a=2.4g,b=1.8g | D. | a<2.4g,b<1.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaCl2 NaCl CaCl2 NaOH | B. | KNO3 NaCl AgNO3 Mg(NO3)2 | ||
| C. | CuSO4 KCl AgNO3 Na2SO4 | D. | BaCl2 CaCl2 KCl Al(NO3)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com