
����Ŀ��ʵ���ҳ��ü��ᣨH2CO2����Ũ�����ϼ����Ʊ�һ����̼����Ӧ����ʽΪH2CO2![]() H2O+CO��������һ����̼��ԭ����ͭ����Ӧ����ʽΪCO+CuO
H2O+CO��������һ����̼��ԭ����ͭ����Ӧ����ʽΪCO+CuO![]() Cu+CO2����ʵ��װ����ͼ��ʾ����ش�
Cu+CO2����ʵ��װ����ͼ��ʾ����ش�
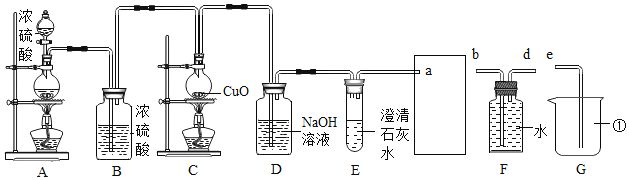
��1��װ��G������������_____��װ��B��������_____��
��2��װ��E����������װ��D���ն�����̼�Ƿ���ȫ����װ��_____����ܡ����ܡ��ﵽĿ�ģ�д��D �еĻ�ѧ��Ӧ����ʽ��_____��
��3��Ϊ����һ����̼��Ⱦ��������������һ����̼��������Ӧ����װ��F��G�����ܽӿڵ�˳��Ϊa��_____��_____��e��
��4����Ӧ�����У�װ��C����ƿ������ͭ��ĩ���ڡ����ڡ�״̬��һ����̼����������£�������������_____����ƿ�ڹ������ʵ���ɫ�仯��_____��
���𰸡��ձ� ��ȥһ����̼�е�ˮ���� ���� 2NaOH+CO2��Na2CO3+H2O d b ��������ͭ�Ӵ���� ��ɫ��Ϊ��ɫ
��������
��1��װ��G�Т����ձ���Ũ���������ˮ�ԣ����Գ�ȥһ����̼�е�ˮ������
��2���ó����ʯ��ˮ�����������̼�Ƿ��������Ҫ������ͨ��ʯ��ˮ�У���������Ӧ����Һ�����£�����ͼʾװ�ò��ܴﵽĿ�ģ�������̼���������Ʒ�Ӧ����̼���ƺ�ˮ��Ӧ�Ļ�ѧ����ʽ�ǣ�2NaOH+CO2��Na2CO3+H2O��
��3��Ϊ���⽫CO�ŷŵ������У�����������CO������Cװ�����ռ�������̼��һ����̼������ˮ���������dz�ˮ�ܣ��ܽӿڵ�����˳��ӦΪa��d��b��e��
��4��װ��C����ƿ������ͭ��ĩ���ڡ����ڡ�״̬����������������ͭ��ĩ��һ����̼����ĽӴ��������Ӧ����֣��ڼ��ȵ������£�һ����̼�ܽ���ɫ������ͭ��ԭΪ��ɫ��ͭ��


 �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ���˫��ˮ��������̻������ȡ������д����ط�Ӧ�Ļ�ѧ����ʽ��___��С��ͬѧ����˫��ˮ�ֽ������Ӱ��������������̽����
��������⣩Ӱ��˫��ˮ�ֽ��������������Щ��
����������裩����һ��������������̵���״�йأ�������������뷴Ӧ�¶��йء�
����Ʋ�ʵ�飩С��ͬѧ��8ml3%��˫��ˮ�Ͷ������̽���������ʵ��(��Ӧ����10sʱ��H2O2����ʣ��)��
ʵ���� | �¶�/�� | �������̵���״(��ȡ0.1g) | �ռ������������/ml(ʱ���Ϊ10s) |
�� | 20 | ��״ | a |
�� | 20 | ��ĩ״ | b |
�� | 20 | ��״ | c |
�� | 20 | ��ĩ״ | d |
(1)��̽���¶ȶ���˫��ˮ�ֽ�������Ƿ���Ӱ�죬Ӧ�ñȽ�___��___(����a����b����c������d��)�Ĵ�С������ĩ״�������̴�Ч���ã���ô___��___(����a����b����c������d��)��
(2)����������ͬ��˫��ˮŨ�ȿ��ܻ�Ӱ���Ч�����������ʵ�鷽��������֤��___��
(3)С��ͬѧ��ʹ����ѹǿ�������ⲻͬ�����������̶�˫��ˮ�ֽ������Ӱ�죬����8mL 3%��˫��ˮ�зֱ������0.03g��0.06g��0.08g��0.12g��0.24gMnO2�����������ѹǿ�ı仯������ͼ��ʾ(���ߵ�б�ʴ���������Ӧ������)������۲�ͼʾ��д�����������Խ��ۣ�
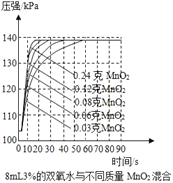
��___��
��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����������ϢϢ��أ���ϵѧ���Ļ�ѧ֪ʶ����Ҫ��������и��⡣
��1����һЩ�ط����ó�ȡ�ĵ���ˮϴ�·�ʱ��������������ĭ�Ҳ�������������ܵ�ԭ���Ǹõ���ˮ��____���Ӳˮ������ˮ������
��2����ʯ��Դúȼ��ʱ���ŷŴ������壬��Щ�����в�����ɿ�����Ⱦ����__________������ĸ��ţ���ͬ����
A CO B CO2 C SO2 D NO2
��3����оƬ�������ܻ������豸�ĺ��IJ���������������Ҫ�Ǹߴ��ȵĵ��ʹ衣�Ʊ��ߴ��ȹ�Ĺ��̽�Ϊ���ӣ�����һ����ѧ��Ӧ�ǣ�SiO2 + 2C = Si + 2CO���÷�Ӧǰ�ϼ۷����ı��Ԫ����_______������Ԫ�����ƣ�
��4��C��H��N����Ԫ�ؿɰ�������6:2:7�γ�һ�ֻ��ȼ��ƫ�����£�����Է�������Ϊ60��ƫ�����µĻ�ѧʽΪ��__________ƫ�������ڿ�������ȫȼ������ˮ����������������Ͷ�����̼���仯ѧ����ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ������ȷ��ӳ��Ӧ�仯��ϵ����

A����������������ơ����������зֱ���������������ϡ����������
B����һ�������Ȼ��������Ȼ����Ļ����Һ�м���þ��������
C����������Ȼ��ƵĻ����Һ����μ��봿����Һ������
D�����������þ�����зֱ���������������ϡ��������ͯ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں�ۡ��ۺͷ���֮�佨����ϵ�ǻ�ѧѧ�Ƶ��ص㡣
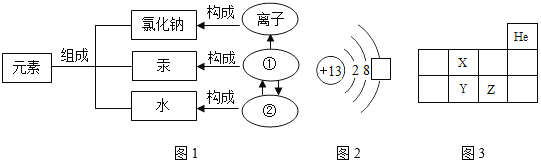
��1�����ʵ���ɼ����ɹ�ϵ��ͼ1��ʾ��ͼ������ʾ����_____������ʾ����_____��
��2������˵����ȷ����_____ ������ĸ����
a �Ȼ��������⡢������Ԫ����ɵ�
b �Ȼ�������������������϶��ɵ�
c �Ȼ�������һ����ԭ�Ӻ�һ����ԭ�ӹ��ɵ�
��3��ͼ2 �����ڵ�������_____����ԭ���γɵ����ӷ���Ϊ_____��
��4���й�ͼ3��˵������ȷ����_____ ������ţ���
a ԭ��������Z��Y b �����������X��Y c Y��Zͬ���ڵڶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʯ��ˮ�����ᷴӦʱ����Һ��pH�仯��ͼ��ʾ����ش�
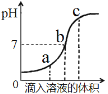
(1)��ʵ���ǽ�___(��ʯ��ˮ��ϡ����)�μӵ���һ����Һ�У��йط�Ӧ�Ļ�ѧ����ʽ��___��
(2)��ͼ��ʾ��a��b��c�����У�___���Ӧ��Һ�к��е�������CaCl2��HCl��___���ʾ�ᡢ��ǡ����ȫ��Ӧ��
(3)����c����Һ�к���Ca(OH)2������ѡ��___(�����)��
��pH��ֽ ��CO2 ��CuSO4��Һ ��Na2CO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�����ڴ�������β������ѧ����ʽΪ��2CO��NH2��2+4X+O2=2CO2+4H2O+4N2����Ӧ������ȥ���������й�˵��������ǣ�������
A. �÷�Ӧ�Ȳ��ǷֽⷴӦҲ���ǻ��Ϸ�ӦB. �μӷ�ӦX����������
C. ���������غ㶨�ɿ�֪X�Ļ�ѧʽΪ![]() D. ��Ԫ���ڷ�Ӧǰ�ϼ۷����仯
D. ��Ԫ���ڷ�Ӧǰ�ϼ۷����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������������е�Ӧ�÷dz��㷺��������ѧ֪ʶ���������ݡ�
��1���Ի���õĹ�������ͭ�Ͻ�����ģ���Ҫ����Ϊͭ�Ͻ���кܺõ�_____������ĸ����
A�������ԡ��� B�������� ����C����չ��
��2��������ʴ����˷ѣ�����Ʒ��ʴ�Ĺ��̣�ʵ��������������е�������ˮ������ѧ��Ӧ�Ĺ��̣�д��һ�ַ����ʩ_____��
��3��Ŀǰ�����ϼ���50%���ϵķϸ����õ��������ã���������_____������ĸ����
A����Լ������Դ ���� B���������ɿ��� ���� C�����ٷϽ����Ի�������Ⱦ
��4����������X��Y���ֽ�����ĩ�ֱ��������ͬ�����ͬŨ�ȵ����ᷴӦ�����������������ʱ��Ĺ�ϵ��ͼ��ʾ������˵���в���ȷ����_____������ĸ����

A��t1ʱ������������������X��Y ���� B��t2ʱ�����Ľ�����������X��Y
C��t3ʱ�����������������X��Y ���� D��t3ʱ�����Ľ�����������X��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����������ʵ��װ��ͼ���ش����⣺
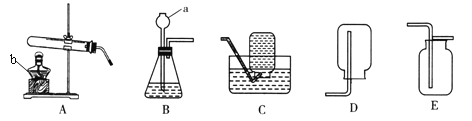
��1��ʵ�����������ƣ�a_______________��b_________________��
��2��ʵ�����ø��������ȡ�����Ļ�ѧ����ʽΪ��________________________________________������װ��Ӧ��ѡ��_______������ţ�����װ����һ�����㣬�������____________________________��Ҫ�ռ����ϴ�����������Ӧ��ѡ��װ��__________������ţ������ø�װ���ռ�������Ҳ������ԭ�������___________��
II��Ϊ̽��̼��ԭ����ͭ�����ʵ����������ľ̿�ۺ�����ͭ�ĸ�������1��2.5g����ϵ��ʵ�顣
���������ϣ�������ͭ��CuO��Ϊ��ɫ���壬����ϡ���ᷴӦ��CuO+H2SO4�TCuSO4+H2O
��̼��ԭ����ͭ�õ���ͭ�п��ܺ���������������ͭ��������ͭΪ��ɫ���壬����ϡ���ᷴӦ��Cu2O+H2SO4�TCuSO4+H2O+Cu��
������ʵ�飩
ʵ��1��ȡ������1��11��ľ̿�ۺ�����ͭ�����1.3g������ʵ�顣
��� | 1��1 | 1��2 |
װ�� |
|
|
��Ӧ�����ʵ���ɫ��״̬ | ��ɫ��ĩ�л���������ɫ���� | ��ɫ�����н��������м�������ɫ���� |
ʵ��2��ȡһ�����Ļ�����1��2װ�ý���ʵ�顣
��� | ľ̿��������ͭ�������� | ��Ӧ�����ʵ���ɫ��״̬ | |
2��1 | 1��9 | ��ɫ�����н������� | ����������ɫ���� |
2��2 | 1��10 | ���к�������ɫ���� | |
2��3 | 1��11 | ���м�������ɫ���� | |
2��4 | 1��12 | ��ɫ���� | |
2��5 | 1��13 | ���н϶��ɫ���� | |
����������ۣ�
��1����̼��ԭ����ͭ�õ��Ĺ���ȫ����ͭ����д����ѧ��Ӧ����ʽ______________________��
��2��ʵ��1��2�У�֤������CO2��������_________________________________________��
��3��ʵ��1��Ŀ����____________________________________________________________��
��4��ʵ��2�Ľ�����______________________________________��
����˼�����ۣ�
��5��ʵ��2û�н���������Ϊ1��14��ʵ�飬������________________________��
��6����μ���2��4�ĺ�ɫ�������Ƿ�Cu2O����д��ʵ�鲽�衢����ͽ��� ________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com