


科目:初中化学 来源: 题型:
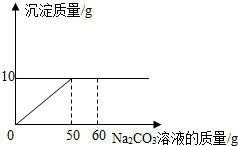 将14.4g由NaCl和CaCl2组成的固体混合物,溶于45.6g的水中,向所得到的混合溶液中逐滴加入质量分数为21.2%的Na2CO3溶液,所加入Na2CO3溶液的质量与产生沉淀的质量关系如图:
将14.4g由NaCl和CaCl2组成的固体混合物,溶于45.6g的水中,向所得到的混合溶液中逐滴加入质量分数为21.2%的Na2CO3溶液,所加入Na2CO3溶液的质量与产生沉淀的质量关系如图:查看答案和解析>>
科目:初中化学 来源: 题型:
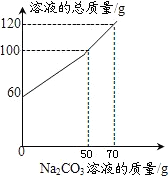 将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图:
将14.4g由NaCl和CaCl2组成的固体混合物溶于水配成60g溶液,向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与所得溶液的总质量关系如图:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
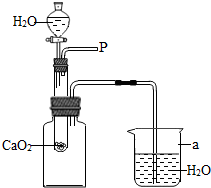 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.| 实验步骤 | 可能出现的现象 | 结论 |
向反应后所得的溶液中通入二氧化碳气体 向反应后所得的溶液中通入二氧化碳气体 |
产生白色沉淀 产生白色沉淀 |
CaO2与H2O反应有Ca(OH)2生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量g | 2.12 | 2.08 | 2.04 | 2.04 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
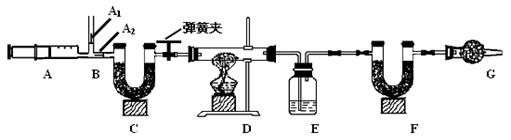
已知:1.碳酸钠比较稳定,加热时不分解;2. 2NaHCO3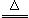 Na2CO3 +CO2 ↑ +H2O
Na2CO3 +CO2 ↑ +H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进
空气,A2关闭。
(一)实验步骤
(1)实验时,组装好装置,实验前应先 ▲ ,然后,实验步骤是:
① 反复推拉注射器 ② 称量E、F的质量 ③ 关闭弹簧夹,加热D处试管直到反
应不再进行 ④ 打开弹簧夹,再次反复缓缓推拉注射器 ⑤ 再次称量E、F的质量。
(二)问题探究:
(2) E中的药品为 ▲ ,E的作用是 ▲ 。
C、F、G中装有碱石灰(生石灰与烧碱的固体混合物),则C的作用是 ▲ ,
F的作用是 ▲ 。
写出 F装置中所发生反应的一个化学方程式 ▲ 。
(3)实验步骤②与③能否颠倒 ▲ (填“能”或“不能”)。若不进行步骤④的操作,
则所测得的碳酸氢钠质量 ▲ (填“偏大”、“偏小”、“无影响”),
该操作中推注射器时缓缓的目的是 ▲ ;
若没有G装置,则碳酸氢钠的质量 ▲ (填“偏大”、“偏小”、“无影响”)。
(4)下表是实验记录数据:
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
则: ① 碳酸氢钠分解生成二氧化碳的质量为 ▲ g
② 碳酸氢钠的质量为 ▲ g
③ 该天然碱的化学式中a:b:c= ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com