
(7分)溶液是生活中常用的混合物。
(1)硫酸铜溶液可用于游泳池消毒,硫酸铜溶液中的溶质是 。
(2)市售的过氧乙酸(CH3COOOH)溶液中溶质的质量分数大多为40%,稳定性差,室温下就可分解成乙酸(CH3COOH),并释放出氧气,该反应的化学方程式为 。将40% 的过氧乙酸溶液稀释成2%,可用于空气消毒, 稀释过程中浓溶液与所加水的质量比为 。
(3)甲、乙两种固体物质的溶解度曲线如图2所示。20 oC时,将等质量的甲、乙分别放入盛有100g水的烧杯中,充分搅拌并升温至50 oC时,实验现象如图1所示。请结合图示回答下列问题:
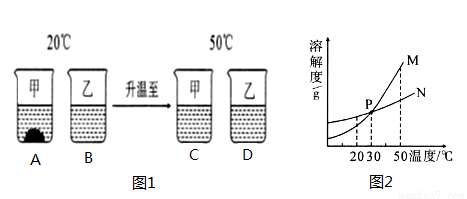
①曲线N表示 (填“甲”或“乙”)的溶解度随温度变化的情况。
②图1所示的四种溶液中,溶质质量分数最小的是 (填字母序号,下同),一定不饱和的是 。
(1)硫酸铜(或CuSO4)
(2)2CH3COOOH = 2CH3COOH + O2↑;1:19
(3)①乙 ②A; CD
【解析】
试题分析:(1)硫酸铜溶液中的溶质是硫酸铜(或CuSO4);
(2)过氧乙酸(CH3COOOH)分解的化学方程式为2CH3COOOH = 2CH3COOH + O2↑;
设将xg40% 的过氧乙酸溶液稀释成2%的过氧乙酸溶液,需要加水yg,则x×40%=(x+y)×2%;x:y=1:19;
(3)①曲线N表示乙的溶解度随温度变化的情况。
②图1所示的四种溶液中,溶质质量分数最小的是A;一定不饱和的是CD。
考点:溶液;化学方程式;溶液中溶质的质量分数;饱和溶液与不饱和溶液。
点评:溶液是由溶质和溶剂共同组成的混合物;
溶质质量分数=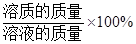 。
。


科目:初中化学 来源: 题型:阅读理解

| 品名:504双吸剂 成分:铁粉、NaCl、炭粉CaO等 |
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源:2013-2014学年江苏省南片七校九年级12月月度调研化学试卷(解析版) 题型:填空题
生活处处皆化学。
(1)生活中的燃烧
①着火点比较:蜂窝煤 小木条(填“>”、“<”或“=”)。生煤炉过程中,不断扇入空气目的是 ,煤不完全燃烧产生一种有毒气体的化学式是 ;
②用水灭火的原理是 ,新型水成膜泡沫灭火剂扑灭油类火灾时,析出的液体和泡沫在油面上铺展形成一层水膜,进而灭火,原理是 。
(2)金属在生活中用途广泛
①下列生活用品,主要是由金属材料制成的是 ;
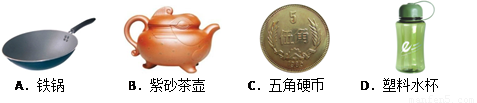
②用铁锅烹饪食物时,会有少量铁屑在胃部(胃酸的主要成分为盐酸)转化为可被吸收的Fe2+,反应的化学方程式为 (2分),是 反应(填基本反应类型)。
③用铝箔包装药物,主要利用了铝的 性;
④铜具有很好的 性,故可作导线。近代湿法冶金的先驱是指 (填化学方程式2分),铜和空气中的O2、H2O及会生成铜锈[Cu2(OH)2CO3],判断的依据是 。
(3)生活中的水和溶液
①处理自然水时,常用的混凝剂是 (填名称)。二氧化氯是一种新型的消毒剂,其化学式为 ;
②欲配制500mL 0.9%的生理盐水(密度为1.0 g/mL),需要NaCl的质量为 g;配制过程中,玻璃棒的作用是 ,称量NaCl时,若将砝码放在左盘(1 g以下用游码),其他操作均正确,则所配溶液中溶质质量分数将 0.9%(填“>”、“<”或“=”)
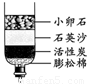
A.净化后的水是纯净物 B.此装置能对水杀菌消毒
C.此装置能把硬水变为软水 D.活性炭能吸附水中的色素及异味
(4)食品包装学问大
①我县特产——荷藕采用真空包装,延长了食品的保质期,原理是 ;
②将N2充入包装袋内做保护气,是因为N2的化学性质 (填“活泼”或“稳定”);
③左图是“504双吸剂”的标签,请问答下列问题:
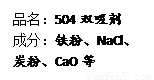
a.其中至少含有 种单质;
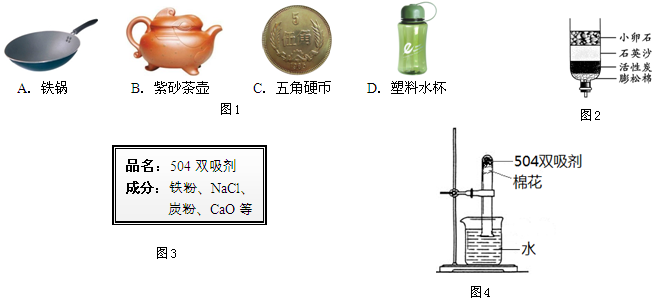
b.为测定此双吸剂的使用效果,取足量双吸剂做了如图所示的实验,一段时间后,进入试管中水的体积 21%(填“>”、“<”或“=”),理由是 ;
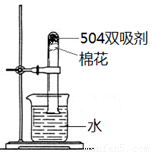
c.部分失效的双吸剂中,有红棕色固体,其主要是 ;
d.此双吸剂中,NaCl的作用可能是 。
查看答案和解析>>
科目:初中化学 来源:2013-2014学年江苏省南片七校九年级12月月度调研化学试卷(解析版) 题型:填空题
生活处处皆化学。
(1)生活中的燃烧
①着火点比较:蜂窝煤 小木条(填“>”、“<”或“=”)。生煤炉过程中,不断扇入空气目的是 ,煤不完全燃烧产生一种有毒气体的化学式是 ;
②用水灭火的原理是 ,新型水成膜泡沫灭火剂扑灭油类火灾时,析出的液体和泡沫在油面上铺展形成一层水膜,进而灭火,原理是 。
(2)金属在生活中用途广泛
①下列生活用品,主要是由金属材料制成的是 ;

②用铁锅烹饪食物时,会有少量铁屑在胃部(胃酸的主要成分为盐酸)转化为可被吸收的Fe2+,反应的化学方程式为 (2分),是 反应(填基本反应类型)。
③用铝箔包装药物,主要利用了铝的 性;
④铜具有很好的 性,故可作导线。近代湿法冶金的先驱是指 (填化学方程式2分),铜和空气中的O2、H2O及会生成铜锈[Cu2(OH)2CO3],判断的依据是 。
(3)生活中的水和溶液
①处理自然水时,常用的混凝剂是 (填名称)。二氧化氯是一种新型的消毒剂,其化学式为 ;
②欲配制500mL 0.9%的生理盐水(密度为1.0 g/mL),需要NaCl的质量为 g;配制过程中,玻璃棒的作用是 ,称量NaCl时,若将砝码放在左盘(1 g以下用游码),其他操作均正确,则所配溶液中溶质质量分数将 0.9%(填“>”、“<”或“=”)

A.净化后的水是纯净物 B.此装置能对水杀菌消毒
C.此装置能把硬水变为软水 D.活性炭能吸附水中的色素及异味
(4)食品包装学问大
①我县特产——荷藕采用真空包装,延长了食品的保质期,原理是 ;
②将N2充入包装袋内做保护气,是因为N2的化学性质 (填“活泼”或“稳定”);
③左图是“504双吸剂”的标签,请问答下列问题:

a.其中至少含有 种单质;
b.为测定此双吸剂的使用效果,取足量双吸剂做了如图所示的实验,一段时间后,进入试管中水的体积 21%(填“>”、“<”或“=”),理由是 ;

c.部分失效的双吸剂中,有红棕色固体,其主要是 ;
d.此双吸剂中,NaCl的作用可能是 。
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
水与人类的生活和生产密切相关。请回答以下相关问题:
 (一)(7分)水——常用的化
(一)(7分)水——常用的化 学试剂
学试剂
(1)作反应物:电解水时, 需在水中加入少量氢氧化钠或硫酸,目的是 ,右图是实验室电解水的微观示意图,其中最小的微粒是 ,通过该实验可以得出的结论是 ;
需在水中加入少量氢氧化钠或硫酸,目的是 ,右图是实验室电解水的微观示意图,其中最小的微粒是 ,通过该实验可以得出的结论是 ;
(2)配制溶液:小丽配制50.0 g 15.0%的氯化钾溶液的操作步骤为:
①计算:需要氯化钾固体的质量为  g;
g;
②称量:用托盘天平称取所需固体。若所用砝码生锈了,则会导致氯化钠溶液的溶质质量分数 (填“<”或“>”)15.0%;
③溶解:该操作中用 (填仪器名称)搅拌至完全溶解;
④装瓶:将配制的溶液倒入 (填“广口瓶”或“细口瓶”),并贴上标签。
(二)(3分)海水——人类的资源宝库
(1)获取淡水:将海水转化为淡水,最常用的操作方法是 ;
(2)获取NaCl:将海水进行 可得到粗盐;为除去粗盐中含有的Na2SO4、CaCl2等杂质,可依次进行下列操作:①溶解;②加过量的BaCl2溶液; ③加过量的Na2CO3溶液;④过滤;⑤加适量的X溶液;⑥蒸发结晶。其中适量X溶液是 (填名称);
(三)(9分)清洁卫生的水——人类需要
(1)下列保护运河水的建议中,合理的是 (填序号);
①生活污水处理后排放; ②将工厂废液排入运河; ③使用无磷洗衣粉;
④减少燃放烟花爆竹; ⑤及时清理运河中疯长的藻类
 (2)以下是污水处理成自来水的工艺流程示意图:
(2)以下是污水处理成自来水的工艺流程示意图:
①污水中含Ca2+、Mg2+、HCO3—等,加入生石灰后生成Ca(OH)2,进而发生若干复分解反应,初级沉降池中生成的主要沉淀是 和 ;(MgCO3微溶于水)
②通入CO2除了能调节自来水的pH,还能 ;
③生物反应池是利用微生物直接分解水中的有机物,以除去水中过多的氮 、磷等有害成分。这样做的优点是 ;
、磷等有害成分。这样做的优点是 ;
④为除去水中悬浮的固体小颗粒,常用的混凝剂是 (填名称);
⑤气体A是 (填化学式),其作用是杀菌消毒,使自来水符合卫生标准,A和H2O反应生成HClO和HCl,写出该反应的化学方程式 ;
⑥饮用含有大量的细菌和杂质的水后,很容易患肠道传染病。请你设计合理方案,将被污染的水处理成能饮用的水: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com