
实验室用大理石与稀盐酸反应制取C02,反应后所得溶
液体积为40 mL(假设大理石中的杂质不与盐酸反应,反应
前后溶液体积不变)。向该溶液中匀速逐滴加入Na2C03溶液
并不断搅拌,测得溶液的pH随时间变化如图所示,该过程
共放出气体660 mL(密度为2.0 g/L),析出沉淀5.090
(1) 根据图像可以看出,Na2C03首先与溶液中的 反应。
(2)本实验制取CO2所用大理石中含CaC03 g。
(3)已知制取C02所用稀盐酸的密度为1.06 g/cm3,求这种盐酸的质量分数。(计算结果保留1位小数,无计算过程不给分)
【答案】(1)HCl(或盐酸)(2)5.0
(3)解:设制取二氧化碳时,与大理石反应的HCl的质量为x,剩余HCl的质量为y
CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
100 73
5.0g x

解得:x=3.65g(1分)
Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
73 44
y 0.66L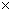 2g/L
2g/L

解得:y=2.19g
盐酸的溶质质量分数为
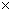 100%=13.8%
100%=13.8%
【解析】(1)从图中,开始时溶液的pH迅速增大,可知,开始时,碳酸钠与盐酸反应;(2)根据质量守恒定律,生成的沉淀是碳酸钠与氯化钙反应所得,反应前后钙元素的质量不变,故生成的沉淀即为原大理石中碳酸钙的质量;(3)利用二氧化碳的质量可计算出与碳酸钠反应的稀盐酸的质量,利用碳酸钙的质量可计算出与与大理石反应的盐酸的质量,两部分盐酸的质量和除以溶液的质量即为盐酸的质量分数。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:初中化学 来源: 题型:
我国大部分地区深受酸雨的危害,煤燃烧产生的SO2是形成酸雨的主要污染物,SO2与水结合生成弱酸性亚硫酸(H2SO3)。
已知:H2SO3易分解生成水和SO2,也易与空气中的氧气或稀硝酸反应生成H2SO4;H2SO3和SO2都能使红色的品红溶液褪色。
(1)酸雨是pH小于________的降雨。
(2)常用脱硫方法减少废气中的SO2,以生石灰(CaO)为脱硫剂,高温下与废气中的SO2与O2化合生成CaSO4,化学方程式为:__________________________________。
(3)实验室常用亚硫酸盐与HCl(或H2SO4)反应制备SO2,Na2SO3与盐酸反应的化学方程式:____________________________。
(4)小鸿同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH,并就反应后混合溶液中的盐成分进行探究:
【提出猜想】反应后的混合溶液中盐的成分是什么?
【进行猜想】猜想1:只有K2SO3;猜想2:____________;猜想3:既有K2SO4,也有K2SO3。
【实验探究】限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、澄清石灰水、品红溶液、紫色石蕊溶液。
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 各取2 mL反应后的混合溶液分别加入A、B两支试管 | — |
| 2 | 向A试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液 | __________________________________________,证明含有K2SO3 |
| 3 | 向B试管中加入__________,再加入足量的__________ | 先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有K2SO4,即猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
生活中常用到各种干燥剂(能除去潮湿物质中水分的物质)。
(1)硅胶是无色或白色颗粒,其主要成分是SiO2,其中Si元素的化合价为_____。
(2)生石灰是白色块状固体,吸水后变成粉末,该反应的化学方程式是_____,该反应可用于自发热饭盒的原因是______。
(3)分子筛干燥剂是铝硅酸盐化合物,其晶体结构中有规整而均匀的孔道,只允许直径比孔径小的分子进入,能吸附水气和其 它气体,吸湿速度极快。分子筛干燥剂吸水前后的变化属于______变化(填“物理”或“化学”)。
它气体,吸湿速度极快。分子筛干燥剂吸水前后的变化属于______变化(填“物理”或“化学”)。
(4)“双吸剂”的主要成分是还原铁粉,常用于食品保鲜,其原因是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
人体注射葡萄糖溶液可以补充能量,葡萄糖(C6H12O6)在体内经缓慢氧化生成二氧化碳和水,释放出能量。若1 000克5%葡萄糖注射液中的葡萄糖完全氧化,计算:
(1)理论上至少消耗O2多少克?
(2)多少升空气中含有这些质量的氧气?
(相对原子质量:H:1、C:12、O:16、O2密度按1.43克/升计,计算结果取整数)
查看答案和解析>>
科目:初中化学 来源: 题型:
现有9.3g NaOH与Na2CO3的固体混合物,测得其中钠元素与碳元素的质量比为23:3。在室温下,将该混合物与50g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为57.1g,则原固体混合物中含有钠元素的质量为下列的( )
A.1.15g
B.2.3g
C.4.6g
D.6.9g
查看答案和解析>>
科目:初中化学 来源: 题型:
下图表示金属活动性顺序中铜、铁和铝被人类大规模开发、利用的大致年限。

(1)分析改图的规律,你认为金属被大规模开发、利用的先后顺序主要与 有关。
(2)科学小组的同学对模拟湿法炼铜实验中得到的铁、铜固体混合物进行含量测定,称取10克固体混合物置于烧杯中,滴加一定质量分数的稀硫酸溶液,记录并绘制了如图所示的曲线。

①10克固体混合物中铜的质量为 克;
②所用稀硫酸溶液溶质的质量分数是多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
小英同学为了侧定某地区石灰石样品中碳酸钙的质量分数,取该样品15g,现将75m1的稀盐酸分三次加人石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
| 实验 | 第一次 | 第二次 | 第三次 |
| 加人稀盐酸的量/ml | 25 | 25 | 25 |
| 生成气体的质量/g | 2.2 | m | 1.1 |
试求:
(1)m的值是 g。
(2)求该样品中碳酸钙的质量分数(保留一位小数)?
查看答案和解析>>
科目:初中化学 来源: 题型:
某混合物中含有碳酸钙和氯化钙,取该混合物6g,向其中加入一定质量的质量分数为10%的稀盐酸,恰好完全反应,产生2.2g气体。(假设气体全部逸出)。
计算:
(1) 所取混合物中碳酸钙的质量。
(2) 所加稀盐酸的质量
(3) 反应后所得溶液中的质量分数(计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
 硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为:FeS2 SO2 SO2 H2SO4
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是 。
②在实验室中不慎将浓硫酸 沾到皮肤上的处理方法是 。
沾到皮肤上的处理方法是 。
A.立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液。
B.立即用稀氢氧化钠溶液冲洗,然后再用水冲洗。
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,沉淀不再产生,问此时液体的pH= 7 (不考虑其它物质的影响),求化工产品中残留Ba(OH)2的质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com