
【题目】为测定某石灰石样品中碳酸钙的含量,取其样品25g,向其中逐滴滴加稀盐酸至无气体生成,加入的稀盐酸与生成的二氧化碳质量关系如下图所示,杂质不溶于水且不与水发生反应,试计算:
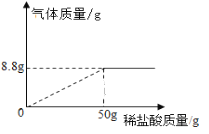
(1)产生气体的质量为____________________。
(2)样品中碳酸钙的质量分数___________。
(3)实验结束后所得溶液的溶质质量分数_____________。
【答案】 8.8g 80% 36.3%
【解析】(1)根据图像解答;(2)(3)根据产生气体的质量求出碳酸钙的质量及生成氯化钙的质量,从而求出样品中碳酸钙的质量分数和溶液中溶质质量分数。(1)由图可知,产生气体的质量为8.8g;
(2)设样品中碳酸钙的质量为x,反应生成氯化钙的质量为y。
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 8.8g
![]()
x=20g
y=22.2g
样品中碳酸钙的质量分数为![]() ×100%=80%
×100%=80%
(3)实验结束后所得溶液的溶质质量分数为![]() ×100%=36.3%
×100%=36.3%
答:(1)产生气体的质量为8.8g;(2样品中碳酸钙的质量分数80%;(3)实验结束后所得溶液的溶质质量分数为36.3%。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具。
⑴用化学符号填空
“雷雨发庄稼”暗含着氮元素在自然界的转化:氮气→一氧化氮→二氧化氮→硝酸。
①两个氮分子___________; ②+2价氮的氧化物__________;
③三个硝酸根离子___________; ④硝酸中氮元素的化合价____________。
⑵用下列字母符号填空
A.碳酸氢钠 B. 漂白粉 C. 生石灰 D.己烷
①.___________可用作食品干燥剂; ②.____________可用作焙制糕点的发酵粉;
③._____________可用作自来水的消毒剂; ④.__________可用作提取大豆中油脂的溶剂。
⑶写出下列反应的化学方程式
①铁在氧气中燃烧: ____________;
②加热氯酸钾制取氧气(用二氧化锰做催化剂): ________________;
③碳酸钠与氢氧化钙溶液反应: _________________;
④铁与硝酸银溶液反应: _________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯氧化钙是用于电子工业的重要无机化工原料,用生石灰(主要成分为CaO)制备高纯氧化钙的工艺流程如下:
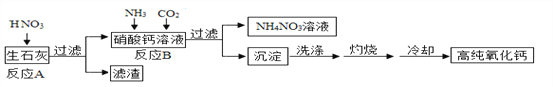
请回答下列问题:
(1)过滤操作中玻璃棒的作用是_______________;
(2)反应B的化学方程式为________________________;
(3)灼烧时发生反应的化学方程式为_________,该工艺流程中可循环使用的物质是_________;
(4)冷却需在密闭和干燥的环境中进行,否则制得的高纯氧化钙中会混有的两种杂质名称分别是___________和__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国自行研发的大型客机C919成功试飞,请根据所学知识回答问题。
(1)选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金的硬度和强度______填“大 于”或“小于”)纯铝;
(2)飞机所用的下列材料属于合成材料的是_____(填序号);
A.塑料扶手 B.纯羊毛毯 C.真皮座套 D.铜制扣件
(3)飞机上的镀铬铁制品能防锈蚀,其防锈原理是阻止了铁与_____接触;
(4)金属铍(Be)与铝化学性质相似,铍元素的核电荷数为4,相对原子质量为9。
①铍原子结构示意图为_____(填序号);
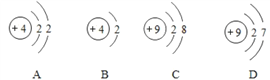
②在空气中,铍的表面易形成一层氧化铍的保护膜,发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图配制溶质质量分数一定的氯化钠溶液请回答下列问题:
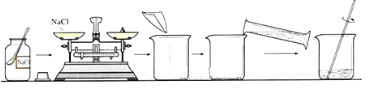
(1)配制氯化钠溶液的操作步骤如下:计算、称量、量取、___________。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏右应 ______ 。(填字母)
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌的目的是_____________
(4)在用量筒量取所需水的过程中,小明俯视读数,这样配得的溶液溶质质量分数会____。(填“偏高”、“偏低”、或“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知草酸(H2C2O4)加热时在浓硫酸的作用下会发生分解反应,某化学兴趣小组对其分解产物进行了如下探究.
(提出猜想)
(1)分解产物是一氧化碳和水蒸气的混合物.
(2)分解产物是二氧化碳和水蒸气的混合物.
(3)分解产物是一氧化碳、二氧化碳和水蒸气的混合物.
你认为合理的猜想是 _________(选填序号),依据是_________。
(查阅资料)
(1)浓硫酸具有脱水性,可以将有机物中的氢、氧元素按水的组成脱去.
(2)白色的无水硫酸铜遇水会变为蓝色.
(3)碱石灰是固体氢氧化钠和氧化钙的混合物.
(进行实验)为了检验草酸的分解产物的成份,小组同学将草酸的分解产物通过下图所示的装置(部分夹持仪器已略去).
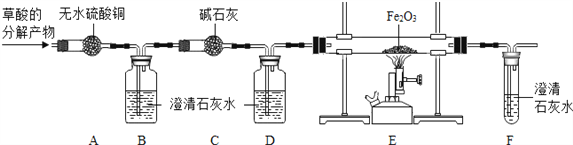
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,证明草酸分解产生了________________ 。
(2)装置D的作用是________________ 。
(3)证明草酸分解产生了一氧化碳的现象应包括_________________.
(4)装置B中发生反应的化学方程式为___________,装置E中发生反应的化学方程式为________.
(得出结论)草酸分解的化学方程式为_________________.
(反思与评价)从环保角度考虑,上述实验的不足之处是____________ .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产氯化钙晶体的流程如下:(原料石灰石中含的杂质主要是MgCO3、MgSO4 和Al2O3)
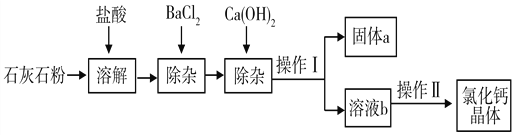
(1)石灰石粉溶解时,Al2O3发生反应的化学方程式为_____________________;
(2)加入BaCl2是为了除去_________________;(填化学式)
(3)操作Ⅱ的具体步骤为___________________ 、冷却结晶;
(4)固体a的成分中含有的物质有_____________________(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】归纳与演绎是重要的科学方法,也是常用的化学学习方法。
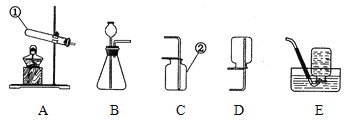
(1)写出标号仪器的名称:①_______________、②______________;
(2)我们已经学过实验室制取O2、H2、CO2三种气体的反应原理,制取与收集方法,请你归纳出实验室制取这三种气体反应的共同点___________(填序号)。
A.需要加热 B.需用催化剂 C.没有气体参加反应 D.生成的气体只有一种
(3)气体发生装置A可用来制取O2,其反应的化学方程式为________________________,可采用______装置来收集该气体。(填序号)
(4)化学上可通过多种反应得到NH3(极易溶于水,密度比空气小),例如:
a.2NH4Cl(固) + Ca(OH)2(固)△CaCl2 + 2NH3↑+ H2O
b.NH4HCO3 (固)△NH3↑+ CO2↑+ H2O c.CaO (固)+ NH3·H2O=NH3↑+ Ca(OH)2
结合以上实验装置完成下列填空: (以下所选装置均填装置序号)
我将选择反应__________(只需选填“a”、“b”或“c”中的一种)作为实验室制取NH3的反应原理,选用上图中的___________作为反应的发生装置,采用的收集装置是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com