
【题目】我们现阶段所学的复分解反应的实质是反应物中的一些阴、阳离子相互结合生成水、气体或沉淀,如BaCl2溶液和Na2SO4溶液反应,实际参加反应的是Ba2+和SO42﹣结合生成BaSO4沉淀,而Cl﹣和Na+则是“旁观者”,并没有参加反应,仍然在溶液中。请在下图圆圈A、B、C、D填入适当的分子或离子符号,体现稀盐酸和碳酸钠溶液反应的实质:
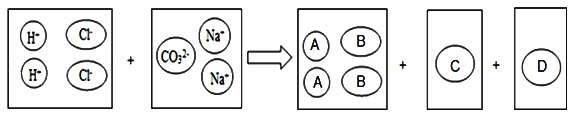
(1)A_____________(2)B_____________
(3)C_____________(4)D_____________
科目:初中化学 来源: 题型:
【题目】如图1所示是实验室制取气体的装置,请回答:
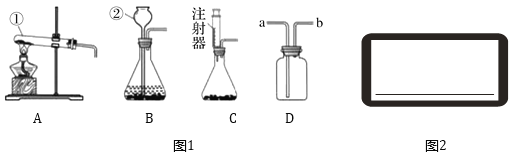
(1)写出有标号仪器的名称:①_________;②_________;
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为________________。若用D装置来收集氧气,气体应从_______(填“a”或“b”)端进入;
(3)在实验室里,二氧化碳常用石灰石与稀盐酸反应来制取.若要控制反应速率和节约药品,应选用的发生装置为_______(填序号);
(4)①用质量分数为37%的浓盐酸配制100g 10%的盐酸,除了用到胶头滴管、玻璃棒和和量筒外,还需补充的一种仪器是___________;
②将上述配制好的溶液装入试剂瓶中,盖好瓶塞并贴上标签。请在如图2所示的标签内填入相应的内容。_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关注健康,预防疾病。下列说法正确的是( )
A. 铝、钡、钛是人体非必需的微量元素
B. 患甲状腺肿大,要多补充些含碘的食物
C. 人体缺氟元素,会得骨质疏松病
D. 缺乏维生素A会引起坏血病
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)图甲是镁原子和氧原子形成氧化镁的示意图
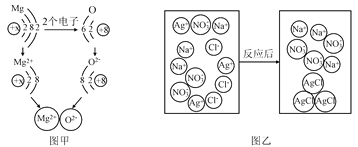
①从得失氧的角度看,镁与氧气的反应属于____ 反应;从得失电子的角度看,反应中镁原子______(填“得到”或“失去”)2个电子,形成相对稳定结构。
②由图甲可知,元素的原子得到电子后,其化合价将______(填“升高”或“降低”)。
(2)图乙是NaCl与AgNO3两溶液反应的示意图。
①图中NO3﹣的名称是______________ 。
②该反应的本质是__________________结合生成沉淀。
③请再用AgNO3作反应物之一,写出另一个与上述反应本质相同的化学方程式:____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师请各小组同学开展探究。
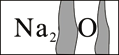
【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里。
由此猜测:这瓶无色溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液。
【理论分析】为了确定该溶液,他们首先进行了分析:
甲同学根据标签上的组成元素认为一定不可能是溶液______________。
乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是__________________。
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验。
实验操作 | 实验现象 |
①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液。 ②静置、过滤,向白色沉淀中滴加__________。 | 产生白色沉淀。 产生大量气泡,沉淀消失。 |
【实验结论】
该瓶无色溶液的溶质是_________,生成白色沉淀的化学方程式是_______________。
【实验反思】
丙同学认为原设计的实验还可简化,同样达到鉴别的目的。丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
实验操作 | 实验现象 |
取少量该无色溶液于试管中,_______________________________________________。 | ______________________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组物质中,均由金属跟同一种酸直接反应生成的是
A. MgSO4和Al2(SO4)3 B. Na2SO4和K2SO3
C. FeCl2和FeCl3 D. ZnCl2和CuCl2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究。
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】为保证实验准确性,实验所用金属片均用砂纸打磨,打磨目的主要是:______________________________。
实验⑴为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡。写出锌与盐酸发生反应的化学方程式为_____________________________。
从实验现象可判断:金属活动性Zn_______Fe(填“<”、“=”或“>”)。
【得出结论1】
金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是_____________________________________________________。
实验⑵为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是__________。
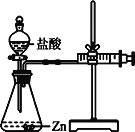
所用药品、实验数据如下表:
实验 编号 | 选用金属 (均取2g) | 盐酸质量分数 (均取50mL) | 每分钟产生氢气的体积/mL | |||||
1分钟 | 1﹣2 分钟 | 2﹣3 分钟 | 3﹣4 分钟 | 4﹣5 分钟 | 前5分 钟共收 集气体 | |||
Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【得出结论2】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是________________。
[注意:若答对下面小题奖励4分,化学试卷总分不超过60分]
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快原因:_________________再由快到慢的原因是_________________。
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?
因素1:_______________________________。
因素2:_______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)请从给定化合价的五种元素![]() 中选择适当的元素,按要求写出相应物质或微粒的符号金属氧化物______;金属单质______;一种酸根离子______。
中选择适当的元素,按要求写出相应物质或微粒的符号金属氧化物______;金属单质______;一种酸根离子______。
(2)下面是4种粒子的结构示意图:
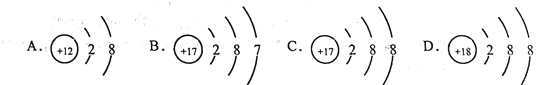
图中粒子共能表示______种元素,表示阳离子的是______ (用离子符号表示),A所表示的元素位于元素周期表的第______周期。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲乙两种固体物质的溶解度曲线。根据图回答问题:
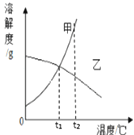
(1)熟石灰的溶解度随温度变化的规律与图中_________(填“甲”或“乙”)相似。
(2)t1℃时等质量的甲、乙两物质的饱和溶液中溶质的质量分数__________填“相等”或“不相等”)。
(3)在大于t1℃时,甲物质的溶解度 _____乙物质的溶解度,小于t1时甲物质的溶解度_____乙物质的溶解度。(均填“大于”或“小于”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com