
| 名称 | 空气中的体积分数(%) | 密度(g/L)(0oC、101.3kPa) | 沸点(℃) | 20°Cl体积水中溶解的体积为 |
| 氮气 | 78.09 | 1.2505 | -195.8 | 0.015 |
| 氧气 | 20.95 | 1.429 | -183.0 | 0.031 |
| 氩气 | 0.93 | 1.784 | -186.0 | 0.035 |
| 二氧化碳 | 0.03 | 1.977 | -78.44 | 0.88 |
分析 由题目的信息可知:氧气在空气中的体积分数为20.95%,氮气在空气中的体积分数是78.09%,密度最大的气体为二氧化碳,密度是1.977g/L,空气中含量最多的气体为氮气;氮气的沸点比氧气的沸点低,因此将完全液化后的空气升高温度,最先气化逸出的气体是氮气.
解答 解:氧气在空气中的体积分数为20.95%,氮气在空气中的体积分数是78.09%,密度最大的气体为二氧化碳,密度是1.977g/L,空气中含量最多的气体为氮气;氮气的沸点比氧气的沸点低,因此将完全液化后的空气升高温度,最先气化逸出的气体是氮气;故答案为:20.95%;二氧化碳;氮气;低;氮气;
点评 本题属于信息题,本考点考查了空气中各种气体的含量,同学们要加强记忆有关的知识点,在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 分子可以构成物质,而原子只能构成分子 | |
| B. | 在化学变化中,分子可以分成原子,而原子不能再分 | |
| C. | 在原子中,质子数等于核外电子数 | |
| D. | 分子是保持物质化学性质的一种粒子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
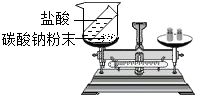 (1)某同学按如图装置对质量守恒定律进行实验探究,反应前天平平衡,然后将稀盐酸倒入烧杯中与碳酸钠充分反应后,再称量,观察到反应后天平不平衡,天平指针向右偏转(填“左”或“右”).该反应遵守质量守恒定律(填“遵守”或“不遵守”).反应后天平不平衡的原因是生成的二氧化碳逸散到空气中使质量减小.
(1)某同学按如图装置对质量守恒定律进行实验探究,反应前天平平衡,然后将稀盐酸倒入烧杯中与碳酸钠充分反应后,再称量,观察到反应后天平不平衡,天平指针向右偏转(填“左”或“右”).该反应遵守质量守恒定律(填“遵守”或“不遵守”).反应后天平不平衡的原因是生成的二氧化碳逸散到空气中使质量减小.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 相等 | B. | 偏小 | C. | 偏大 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲>乙>丙 | B. | 乙>甲>丙 | C. | 甲>丙>乙 | D. | 丙>甲>乙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 2.2 | 6.4 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 3.6 | 2.2 | a |
| A. | 表中a的值为5.6 | B. | X中含有氧元素 | ||
| C. | X由碳、氢两种元素组成 | D. | X可能是该反应的催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲>乙>丁>丙 | B. | 丙>丁>乙>甲 | C. | 丙>乙>丁>甲 | D. | 乙>丁>甲>丙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 炒菜时油锅着火,可立即加水灭火 | |
| B. | 夜晚发现液化气泄漏不应立即开灯检查 | |
| C. | 人们每天的饮食中都应有蔬菜、水果,其目的是补充维生素 | |
| D. | 扑灭电器、图书档案等火灾最适宜的灭火器是液态二氧化碳灭火器 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com