
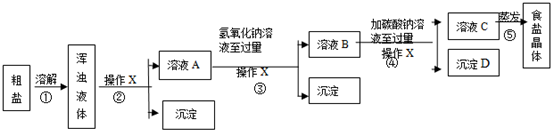
分析 根据物质除杂的方法进行分析解答,根据过滤需要的仪器进行解答;氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠;碳酸钠能与氯化钙反应生成碳酸钙沉淀和氯化钠,加入盐酸可以除去过量的氢氧化钠和碳酸钠,据此解答.
解答 解:(1)据图可以看出,实验操作X得到了固体和用途,故其操作的名称是过滤,该操作中要用到的玻璃仪器有烧杯、玻璃棒和漏斗,故填:过滤,漏斗.
(2)实验步骤③加入的氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠,其主要目的是除去氯化镁;判断氢氧化钠溶液已过量的方法是加入酚酞,溶液变红,取少量的溶液B,滴加酚酞试液,溶液变成红色;故填:2NaOH+MgCl2═Mg(OH)2↓+2NaCl;取少量的溶液B,滴加酚酞试液,溶液变成红色.
(3)实验步骤④中加入的碳酸钠能与氯化钙反应生成碳酸钙沉淀,故填:CaCO3.
(4)由于加入的氢氧化钠和碳酸钠都是过量的,所以溶液中会残留着二者,因此最后得到的氯化钠也不是纯净的,因此实验方案不完善,故填:加入的氢氧化钠和碳酸钠都是过量的,所以溶液中会残留着二者,因此最后得到的氯化钠也不是纯净的.
(5)为了完善原实验方案,需要加入盐酸除去过量的氢氧化钠和碳酸钠,可以加入盐酸至没有气泡产生停止,故填:在操作④中加入盐酸,至恰好没有气泡冒出后就停止加入.
点评 本题考查的是粗盐提纯的知识,完成此题,可以依据已有的知识进行.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐酸是混合物,其溶质是一种气体 | |
| B. | 盐酸和氢氧化钠溶液反应放出大量的热 | |
| C. | 浓盐酸敞口放置一段时间后,溶质的质量分数会变大 | |
| D. | 若有很少量的稀盐酸不慎沾到皮肤上,应立即用较多的水冲洗 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com