
| A. | Fe,Hg | B. | Fe,Zn | C. | Cu,Hg | D. | Cu,Zn |
分析 根据题意,X、Y两金属都能与AgNO3溶液反应,置换出Ag,说明X、Y两金属的活动性均比银强;X跟H2SO4不反应,Y跟H2SO4反应生成H2,说明X的金属活动性比氢弱,Y的金属活动性比氢强;即Y>H>X>Ag,据此进行分析判断.
解答 解:X、Y两金属都能与AgNO3溶液反应,置换出Ag,说明X、Y两金属的活动性均比银强;X跟H2SO4不反应,Y跟H2SO4反应生成H2,说明X的金属活动性比氢弱,Y的金属活动性比氢强;即Y>H>X>Ag.
A、铁排在氢的前面,不符合H>X,故选项错误.
B、铁排在氢的前面,不符合H>X,故选项错误.
C、铜排在氢的后面,汞排在氢的后面,不符合Y>H>X,故选项错误.
D、铜排在氢的后面,锌排在氢的前面,符合Y>H>X>Ag,故选项正确.
故选:D.
点评 本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.


科目:初中化学 来源: 题型:解答题
| KNO3 | Ca(NO3)2 | Na(NO3)2 | Mg(NO3)2 | Al(NO3)3 | Zn(NO3)2 | Fe(NO3)2 |


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
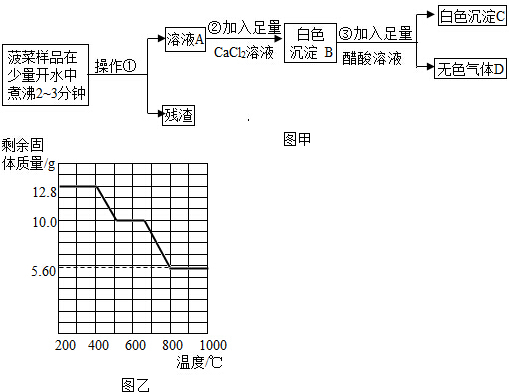
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 莽草酸中氢元素的质量分数最大 | B. | 莽草酸由碳、氢、氧三种元素组成 | ||
| C. | 莽草酸中各元素的质量比为7:10:5 | D. | 每个莽草酸分子里含有5个氢分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
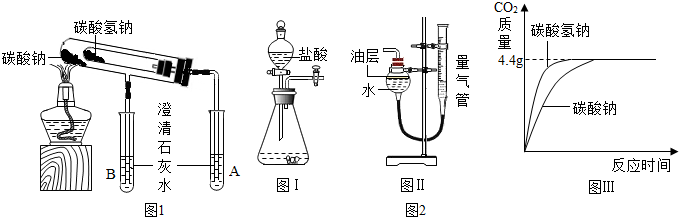
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | B>A>C | B. | A>B>C | C. | B>C>A | D. | C>A>B |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化分解 | B. | 合成新的自身蛋白质 | ||
| C. | 合成脂肪 | D. | 以上三者都不是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com