

分析 (1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(2)铁在有水和氧气并存时易生锈;
(3)从废液中含有氯化钠、氯化铜和氯化亚铁,到产品中有铜(Cu)和氧化铁两种产品,找到废液中成分与产品之间的关系入手,从而找出A、B、G的成分.
充分利用题目给出的信息:“过程中不引入其他元素”,根据关系可知C为稀盐酸,要想证明稀盐酸过量,可从酸的化学性质来解答.
解答 解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)铁在有水和氧气并存时易生锈,故填:与水和氧气共存;
(3)①由于题目中指出:“某课外小组利用废液制取海绵铜(Cu)”,而“工厂废液中含有氯化钠、氯化铜和氯化亚铁.”根据质量守恒定律可知,要想制取铜,就要把氯化铜中的铜置换出,而题目中又明确指出不得加入其他元素,只能选择题目中氯化钠、氯化铜和氯化亚铁含有的金属元素组成的单质.”三种物质中含有氯元素、钠元素、铜元素、铁元素中,符合题意的可组成的金属有钠和铁.钠的活动性又太活泼,可以和水反应,故不能用来置换氯化铜溶液中的铜;铁则可以和氯化铜溶液反应,生成氯化亚铁和铜,反应的化学方程式为:Fe+CuCl2═FeCl2+Cu,为使废水中的氯化铜完全反应,就加入过量的A(铁);由于加入是过量铁,由铁有剩余,故固体B的成分为剩余的铁和生成的铜;要获得产品铜就要除去剩余的铁,由于在金属活动顺序表中铁位于氢之前而铜位于氢之后,铁可和稀盐酸反应(Fe+2HCl═FeCl2+H2↑),而铜不反应,故可在固体B中加入足量的稀盐酸,由此确定产品F为铜,另一种产品G则只能是氧化铁.D中的溶质是氯化钠和氯化亚铁;故填:氯化钠和氯化亚铁;
②由分析①中可知C为稀盐酸,想证明溶液中含有稀盐酸,可利用酸的化学性质:①和酸碱指示剂反应②和活泼金属反应③和金属氧化物反应④和碱反应⑤和盐反应中的一种即可,如可利用和活泼金属的反应:取少量溶液E于试管中,向其中加入适量的铁粉,若有气泡产生,则盐酸过量;故答案为:取少量溶液E于试管中,向其中加入适量的铁粉,若有气泡产生,则盐酸过量(其他合理也可).
点评 考点考查了物质的制备,物质的制备有一下几种类型:一种是只能用题目给出的原料来制取;一种是自己选取原料来制备新物质;还有的是给你一部分药品,其它自选等.本题结合物质的性质,灵活应用,答案就会迎刃而解.


科目:初中化学 来源: 题型:实验探究题
 某同学设计如图所示的装置.将铁丝放在潮湿的空气中,一周后,除观察到铁丝生锈,还观察到的现象是烧杯中的水沿导管上升;打开K后,观察到铁锈消失,写出该反应的化学方程式Fe2O3 +6HCl=2FeCl3+3H2O;随着盐酸的滴加,过一会观察到烧杯内的导管口有气泡冒出,请解释产生该现象的原因盐酸和铁反应生成生成氢气,从导管口逸出.
某同学设计如图所示的装置.将铁丝放在潮湿的空气中,一周后,除观察到铁丝生锈,还观察到的现象是烧杯中的水沿导管上升;打开K后,观察到铁锈消失,写出该反应的化学方程式Fe2O3 +6HCl=2FeCl3+3H2O;随着盐酸的滴加,过一会观察到烧杯内的导管口有气泡冒出,请解释产生该现象的原因盐酸和铁反应生成生成氢气,从导管口逸出.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 物质 | Al(OH)3 | NaAlO2 | AlCl3 |
| 溶解性 | 不溶 | 溶 | 溶 |
| 实验步骤 | 预期实验现象 | 预期实验结论 |
组装下图装置进行实验.取少量摩擦剂于锥形瓶中,加入适量的稀盐酸.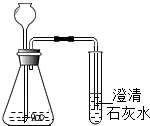 | 固体全部溶解,有气泡,石灰水变混浊 | 则猜想1成立 锥形瓶中发生的化学反应方程式为Al(OH)3+3HCl=AlCl3+3H2O CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 摩擦剂部分溶解 石灰水无明显变化 | 则猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盛装溶液的试剂瓶中有少量10%的氯化钠溶液 | |
| B. | 称量氯化钠固体时所用天平的砝码缺了一个角 | |
| C. | 用量筒量取水时俯视读数 | |
| D. | 将称量好的氯化钠固体倒入烧杯中时,有部分氯化钠固体散落在实验桌上 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钠 | B. | 生石灰 | C. | 浓硫酸 | D. | 硝酸铵 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 一天,实验助手小林走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
一天,实验助手小林走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com