
【题目】硫酸钙转化为K2SO4和CaCl2.6H2O的工艺流程如下图:
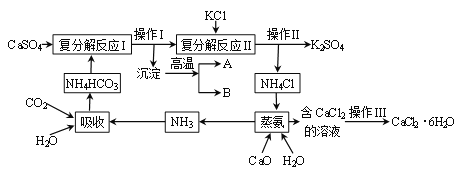
⑴吸收过程中发生了化合反应,化学方程式为__________________ 。
⑵操作Ⅰ的名称为__________,请完成复分解反应I的反应化学方程式:CaSO4 + 2NH4HCO3==== (NH4)2SO4 +________↓+H2O + CO2↑
⑶蒸氨过程中涉及的反应类型___________(填编号)
A 复分解反应 B 化合反应 C 分解反应 D 置换反应
⑷ 操作Ⅲ包含一系列操作:蒸发浓缩、_______________、过滤、洗涤、干燥。
⑸可循环利用的物质除NH3外,还有______________(填化学式)。
⑹若原料CaSO4的质量为68g,理论上可得到产品K2SO4的质量为_____g。
【答案】 CO2 + H2O + NH3 === NH4HCO3 过滤 CaCO3 AB 降温结晶 CO2 CaO 87
【解析】(1)在吸收过程中,氨气、水和二氧化碳发生了化合反应生成了碳酸铵,反应的方程式是:CO2+H2O+2NH3=(NH4)2CO3;(2)碳酸铵与硫酸钙反应生成了碳酸钙沉淀和硫酸铵,是固液混合物,利用过滤的方法将它们分开;所以,操作I的名称为过滤,沉淀的主要物质为CaCO3;(3)在蒸氨过程中,氧化钙与水化合生成了生成了氢氧化钙,反应是:CaO+H2O═Ca(OH)2;该反应有两物质生成了一种物质,属于化合反应.氢氧化钙与氯化铵反应反应生成了氯化钙、氨气、水,反应方程式是:2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑,该反应有两种化合物相互交换成分生成了两种新的化合物,属于复分解反应.所以,AB正确,CD错误;(4)从氯化钙溶液中结晶析出CaCl2?6H2O,需要:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;(5)由硫酸钙转化为K2SO4和CaCl2?6H2O的工艺流程中涉及到的物质可知,NH3外,CO2CaO可以可循环利用;⑹据质量守恒定律可知反应前后元素种类、质量不变,若原料CaSO4的质量为68g,理论上可得到产品K2SO4的质量为:
68g×![]() ÷
÷![]() =87g。
=87g。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下图是氯化钠和碳酸钠在水中的溶解度曲线,下列说法正确的是
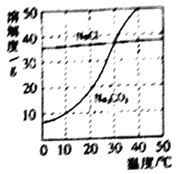
A. 两种物质都属于易溶物质
B. 碳酸钠的解度比氯化钠的溶解度受温度的影响较小
C. 降温结晶可除去氯化钠中含有的少量碳酸钠
D. 氯化钠的溶解度大于碳酸钠的溶解度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于反应类型和物质类别的判断不完全正确的是( )
选项 | 化学方程式 | 反应类型 | 所选物质类别 |
A | FeCl3+3NH3H2O=Fe(OH)3↓+3NH4Cl | 复分解反应 | NH3H2O是碱 |
B | 3C+2Fe2O3 | 置换反应 | Fe是金属单质 |
C | 4NO2+O2+2H2O═4HNO3 | 化合反应 | HNO3是酸 |
D | 2KClO3 | 分解反应 | KClO3是氧化物 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关于反应C + 2H2SO4(浓)![]() CO2↑+ 2X↑+2H2O 。下列分析错误的是
CO2↑+ 2X↑+2H2O 。下列分析错误的是
A. X的化学式为SO2
B. 该反应生成的CO2和X的质量比为1:2
C. X气体排放到空气中,会造成空气污染
D. 碳元素的化合价在反应前后由0价变为+4价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关化学反应类型的判断,错误的是
选项 | 化学方程式 | 反应类型 |
A | 4Fe(OH)2+O2+2H2O = 4Fe(OH)3 | 化合反应 |
B | 2NaHCO3 | 分解反应 |
C | BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2 | 复分解反应 |
D | Fe3O4+4CO | 置换反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学用语书写正确的是
A. 三个二氧化硫分子:2SO3 B. 两个氮分子:2N
C. HClO中氯元素的化合价:![]() D. 一个铝离子:Al+3
D. 一个铝离子:Al+3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。可以说镍行业发展蕴藏着巨大的潜力。
Ⅰ制备草酸镍
工业上可利用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍(NiC2O4)。
根据下列工艺流程图回答问题:
【资料卡片1】
(1)过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢具有强氧化性,所以常作为氧化剂、漂白剂和消毒剂。
(2)氧化反应可以从元素化合价升降的角度进行分析:物质所含元素化合价升高的反应就是氧化反应。
(3)金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。
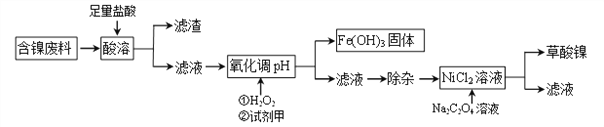
(1)“酸溶”之后的滤渣中含有的金属是_______________。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式_________________________。
(3)加H2O2时,温度不能太高,其原因是_______________________。若H2O2在“酸溶”步骤即与盐酸同时加入,则与原方案相比滤液中会增加的金属离子是Cu2+和_______(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式____________。
Ⅱ制备镍粉
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3yNi(OH)2zH2O,并利用其制备镍粉,过程如下:
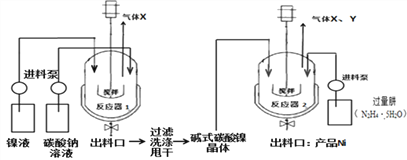
(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O ![]() NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体已洗涤干净的试剂是____________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是_________(填名称)。
Ⅲ 测定碱式碳酸镍晶体的组成
为测定碱式碳酸镍晶体【xNiCO3yNi(OH)2zH2O】组成,某小组设计了如下实验方案及装置:
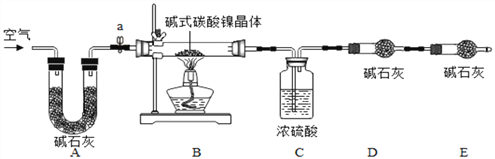
【资料卡片2】
(1)碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(2)在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3
(3)碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
【实验步骤】
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体【xNiCO3yNi(OH)2zH2O】放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 201.08 | 180.44 | 180.00 |
【实验分析及数据处理】
(9)计算3.77g碱式碳酸镍晶体【xNiCO3yNi(OH)2zH2O】中镍元素的质量_________(写出计算过程,计算结果准确到小数点后两位)。
【实验反思】
(10)另一小组同学在实验中发现,实验结束后,称得装置B中残留固体质量明显偏大,老师带领全组同学经过仔细分析后发现,这是由于该组同学加热时在酒精灯上加了铁丝网罩,温度过高所导致。请问该组同学称得的残留固体中镍元素的质量分数可能是__________。
A.70.08% B.75.88% C.78.67% D.79.58%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家最新发现,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如下。 下列说法正确的是

A. 反应前后分子总数不变
B. 反应中 X、Z 两种物质的质量比为 3:7
C. 反应中 Y 和 W 的物质的量之比为 4:5
D. 参加反应的 Y 中氮元素的质量一定等于生成 Z 的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类生活生产离不开金属,请回答下列问题:
(1)下列现象和事实,不.可.以.用金属活动性作合理解释的是__________。
A.金属镁在空气中比铝更容易燃烧, 说明镁比铝的活动性强
B.金属铝比金属锌更耐腐蚀, 说明锌比铝活动性强
C.用硫酸铜、生石灰加水配制农药波尔多液时,不能用铁制容器
D.金属的种类很多,但在自然界中,仅有少数金属如金、银等有单质形式存在
(2)某小组用如下图所示装置对铁生锈的条件进行探究,四分钟后发现 A 中铁钉表面灰暗,B 中铁钉依然光亮,对比 A、B 现象说明:决定铁生锈快慢的一个重要因素是____。
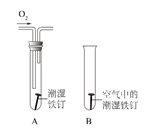
(3)多数金属以矿物形式存在于自然界,金属矿物可以用来冶炼金属。
①高炉炼铁的原料主要是铁矿石、______、石灰石、空气。工业上常用赤铁矿(主要成分是Fe2O3)在高炉中炼铁,反应的化学方程式是___________ 。
②我国古代将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到 800℃, 得到貌似金 子的铜锌合金,反应原理如下,试补充完成其中的另外两个化学方程式。
A.ZnCO3=ZnO+CO2↑
B.C+2Cu2O=_____________+CO2↑
C.____________________
(4)将mgZn和Fe的混合物中加入一定质量的CuCl2,充分反应后过滤,将滤渣洗涤, 干燥后称量质量仍为 mg,对所得滤液和滤渣的判断不正确的是_____________。
A.滤液中一定有ZnCl2和FeCl2 B.滤液为无色
C.滤渣中只有铜 D.滤渣中加稀盐酸一定有气泡产生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com