
下列图示实验操作中,不正确的是( )
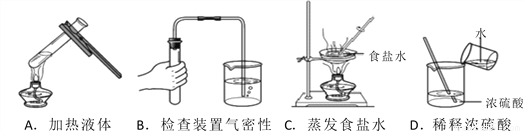
A. A B. B C. C D. D
D 【解析】A.加热液体。故A正确。B.检查装置气密性。故B正确。C.蒸发食盐水。故C正确。D.稀释浓硫酸,浓硫酸应倒入水中。故D错误。 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:初中化学 来源:四川省绵阳市游仙区2018届九年级下学期二诊化学试卷 题型:综合题
(1)某兴趣小组准备通过锌与稀硫酸反应产生的氢气来测定稀硫酸中溶质的质量分数,装置如下:

①小明同学用如图1所示装置进行实验,你认为他应该选择的最简易的装置及其连接顺序是:A→______→ D。
②小明若用图2装置收集氢气,应选择集气装置____(填“A”或“B”),为保证测量结果的准确性,收集气体的时机是_________。
a.导管口还没有气泡产生时
b.导管口连续均匀冒出气泡时
c.导管口冒出气泡很多时
③小张同学用如图3所示装置进行了实验:
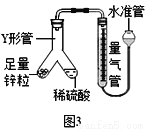
Ⅰ.下列能说明装置气密性良好的是_________。
A.连接仪器后,向水准管中注水,直至左右两边管内形成稳定高度差。
B.向水准管内注水,连接好左侧装置,抬高水准管,左右两边液面始终相平。
Ⅱ.反应完毕后,每间隔1分钟读取气体体积、气体体积逐渐减小,直至体积不变。气体体积逐渐减小的原因是_________________(排除仪器和实验操作的影响因素)。
Ⅲ.若实验中测得稀硫酸的溶质质量分数偏大,下列可能的原因是____________。
a.装置漏气 b.读取数据时水准管的水面高于量气管的水面
c.未待冷却就读取量气管读数
(2)在金属活动性顺序表中,排在前面的金属能把位于后面的金属从它的盐溶液中置换出来,但小明在做金属钠与硫酸铜溶液反应的实验时,却出现了异常现象。
【进行实验】取一块绿豆大小的金属钠,放入盛有20毫升硫酸铜溶液的小烧杯中,发现金属钠浮在液面上不停打转,产生大量气体,烧杯发烫,溶液中出现了蓝色絮状沉淀,一会儿部分沉淀渐渐变黑,将反应后烧杯中的混合物进行过滤,得滤渣和无色滤液。
【提出问题】①生成的气体是什么?
②滤渣的成分是什么?
③无色滤液中的溶质是什么?
【查阅资料】①钠能与水反应生成一种碱,同时放出气体。
②氢氧化铜受热至60~80℃变暗,温度再高分解为相应的金属氧化物(化合价不变)和水。
【实验探究一】 探究生成的气体是什么?
小明将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,把气体通入肥皂水中,将燃着的木条靠近飘起的肥皂泡,有爆鸣声。说明生成的气体是___________。
【实验探究二】 探究滤渣的成分是什么?
【猜想假设】滤渣中含有Cu(OH)2和_____________,还可能含有Cu。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量滤渣,向其中加入足量的稀硫酸 | ____________________ | 滤渣中没有Cu |
【实验结论】通过实验,小明同学得出结论:钠加入到硫酸铜溶液中会先与水反应,生成物再与硫酸铜反应生成氢氧化铜。请写出上述发生的两个反应的化学方程式______________ ,________________。
【实验探究三】探究无色滤液的溶质是什么?
【猜想假设】猜想① Na2SO4 , 猜想②________________。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量无色滤液,向其中加入__________ | 无明显变化 | 猜想①成立 |
【反思交流】钠加入硫酸铜溶液中出现黑色物质的可能原因是(用化学方程式表示)_________。
C B a A 反应放热、气体在冷却过程中体积逐渐减小 c H2 CuO 固体全部溶解、溶液变成蓝色 2Na + 2H2O = 2NaOH + H2↑ CuSO4+2NaOH = Cu(OH)2↓+Na2SO4 Na2SO4和NaOH 无色酚酞试液 Cu(OH)2CuO + H2O 【解析】①最简易的装置及其连接顺序是:A→C→ D。用C收集氢气,同时通过读取压入D中水的体积,测定收集到氢气...查看答案和解析>>
科目:初中化学 来源:山东省泰安市岱岳区2017-2018学年八年级下学期期中考试化学试卷 题型:单选题
保护地球、防止环境污染是我们的重要职责,合理利用资源是保护地球的重要途径,下列关于资源利用的说法中,错误的是
A. 减少煤炭资源的过度开采
B. 积极开发太阳能
C. 倡导“低碳生活”,绿色出行
D. 为方便出行,提倡多开私家车
D 【解析】A、化石燃料包括煤、石油和天然气,属于不可再生能源,且面临着被耗尽的危险,应合理开采,正确;B、太阳能是清洁能源,积极开发太阳能可以节约化石能源,减少空气污染,正确;C、倡导“低碳生活”,绿色出行,可以节约能源,减少空气污染,正确;D、提倡多开私家车出行,会浪费化石能源,加重空气污染,错误。故选D。查看答案和解析>>
科目:初中化学 来源:江苏省2018届九年级第二次模拟考试化学试卷 题型:多选题
H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示(mol·L-1是浓度的一种表示方法)。下列说法正确的是
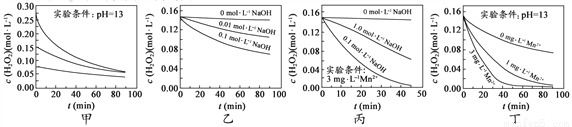
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液pH越大,H2O2分解速率越快
C. 图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丁表明,碱性溶液中,Mn2+浓度越大,H2O2分解速率越快
BD 【解析】A. 图甲表明,其他条件相同时,H2O2浓度越大,其分解速率越快,错误;B. 图乙表明,其他条件相同时,溶液pH越大,H2O2分解速率越快,正确;C. 由图丙可知,少量Mn 2+存在时,1.0mol·L-1 NaOH条件下对应的H2O2分解速率要小于0.1mol·L-1 NaOH时的分解速率,因此并不是碱性越强,H2O2分解速率越快,错误;D. 图丁表明,碱性溶液中,Mn2+浓...查看答案和解析>>
科目:初中化学 来源:江苏省2018届九年级第二次模拟考试化学试卷 题型:单选题
下列做法,不正确的是( )
A、用灼烧的方法区分羊毛和涤纶
B、用肥皂水区分硬水和软水
C、用品尝的方法区分糖水和火碱水
D、用碘水区分奶粉和淀粉
C 【解析】 试题分析:火碱水即氢氧化钠,有强腐蚀性,不能品尝,C错误。查看答案和解析>>
科目:初中化学 来源:四川省成都市成华区2018届九年级二诊考试化学试卷 题型:科学探究题
某校化学活动小组用镁和铁探究金属的反应规律。
【查阅资料】
①镁,铁的活动性均在 H 之前并且镁比铁活泼。
②相同条件下,相同时间内金属的活动性越强,与酸反应越剧烈,产生的氢气越多。
【探究一】在室温条件下进行如图所示实验。试管内的镁带和铁片表面均被打磨洁净,且形 状、大小相同;同时加入等质量和等浓度的稀盐酸。
(1)该兴趣小组的同学认为该方案中长颈漏斗起非常重要的作用。
①通过相同条件下,相同时间内长颈漏斗中 __________
②长颈漏斗在实验中还可以起_________________ 作用。
(2)在甲、乙装置的水中滴入 2~3 滴红墨水的目的_______________。
(3)乙装置中反应方程式为______________,该反应属于基本反应类型中的_______反应。
(4)观察到甲装置中产生气泡速率比乙装置快或 __________现象时,都可以证明镁的金属活动性比铁的强。
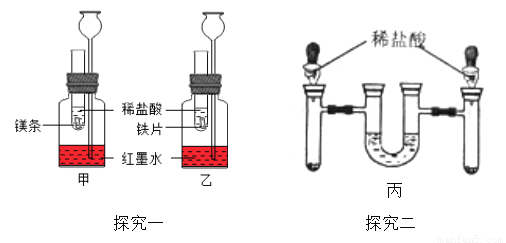
【探究二】方案二:如图丙,将等质量光亮洁净,形状厚薄相同的镁条和铁片分别放入左、 右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U 型管内为水,初始液面相平,反应过程中装置气密性良好)。
(5)实验过程中 U 型管中液面 _______(填“左高右低”,“左低右高”,“相平”); 充分反应后,冷却到室温 U 型管中液面 ___________填“左高右低”,“左低右高”,“相平”),原因是_____。
【探究三】在硫酸铜和硫酸亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出 的固体中滴加稀硫酸,没有气泡产生。下列判断正确的是 ________。写成发生反应的化学方程式 ________ 。
A.滤出的固体中一定含有铜 B.滤出的固体可能含有铁和镁
C.滤液中可能含有硫酸铜 D.滤液中一定含有硫酸镁和硫酸亚铁
液面的高低 平衡内外压强 便于观察实验现象 Fe + 2HCl = H2↑ + FeCl2; 置换 甲中长颈漏斗的液面比乙中高 左低右高 ; 相平; 金属均有剩余,充分反应后生成的 H2 质量相等 A,B ; Mg + CuSO4 = Cu + MgSO4 【解析】镁和铁探究金属的反应规律。镁,铁的活动性均在 H 之前并且镁比铁活泼,镁和铁均可与盐酸或硫酸反应。相同条件下,相同时间内金属的活...查看答案和解析>>
科目:初中化学 来源:四川省成都市成华区2018届九年级二诊考试化学试卷 题型:单选题
下列有关能源和环保的说法正确的是
A. 天然气是可再生能源
B. 氢能是目前最经济、最安全的能源
C. 煤完全燃烧后不会对环境造成污染
D. 太阳能、潮汐能、风能是人类正在利用和开发的重要能源
D 【解析】A、天然气是不可再生能源,故A错误;B、氢能是目前最经济、最环保的能源,不纯容易引起爆炸,故B错误;C、煤含有硫等多种杂质,完全燃烧后会对环境造成污染,硫燃烧生成二氧化硫,二氧化硫属于大气污染物,故C错误;D、太阳能、潮汐能、风能是人类正在利用和开发的重要能源,无污染,故D正确。 点睛∶煤,石油和天然气都属于不可再生资源,特别是煤和石油燃烧会对环境造成污染。氢气燃烧虽然环保...查看答案和解析>>
科目:初中化学 来源:广东省广州市毕业班综合测试化学试卷 题型:科学探究题
食盐(NaCl)、碳酸钠(Na2CO3)、生石灰(CaO)是制作皮蛋料泥的主要原料。制作料泥时,将上述原料加入适量水中,搅拌混合均匀即可。
(1)①制作料泥时,生石灰与水反应的化学方程式是__________________。
②制作料泥时,与碳酸钠反应的物质是_____________________(写化学式)。
(2)某化学兴趣小组对影响溶液碱性强弱的因素展开探究。用不同温度的水,配制溶质质量分数分别为2%、6%和10%的碳酸钠溶液,依次测量溶液的pH,记录数据如下表:
实验编号 | a1 | a2 | a3 | b1 | b2 | b3 | c1 | c2 | c3 |
溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
水的温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 50 | 70 |
溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | X | 11.50 |
请你分析表中数据回答:
①溶液碱性最强的是___________(填实验编号)
②实验a1、b1、c1的实验目的是________________________。
③在相同的条件下,一定温度范围内,温度与碳酸钠溶液pH的关系是____________________。
④表格中X的数值可能是____________(填选项)。
A.11.20 B.11.25 C.11.37 D.11.62
CaO + H2O = Ca(OH)2 Ca(OH)2 c3 在相同的条件下(在水温相同时),探究碳酸钠溶液的溶质质量分数对溶液pH的影响 温度越高,碳酸钠溶液的pH越大 C 【解析】(1)①氧化钙与水反应生成氢氧化钙,反应方程式为CaO + H2O = Ca(OH)2; ②氧化钙与氢氧化钠反应生成的氢氧化钙可以与碳酸钠反应生成碳酸钙沉淀,故可以与碳酸钠反应的是氢氧化钙,化学式为Ca(...查看答案和解析>>
科目:初中化学 来源:广西壮族自治区钦州港经济技术开发区中学2018届春季3月份考试化学试卷 题型:简答题
锁是日常生活中常用的工具,其中的铁锁经常会生锈。
(1)铁锁在哪种情况下使用易生锈 铁锁的各个部分通常采取了怎样的防锈措施 (举两个不同部位的不同措施) _____________________
(2)如果锁芯因生锈转动时有些不灵活,可以向锁芯中注入哪种无机物使之转动灵活。
________
雨淋(或在潮湿空气中,或接触酸碱盐的溶液等) 锁身通常喷漆;锁勾通常是不锈钢或镀铬镍 注入铅笔芯粉末(石墨粉) 【解析】:(1)铁锁在雨淋时易生锈,为防止铁锁生锈,锁身通常采用喷漆的方法,锁勾采用镀铬或镍的方法,所以本题答案为:雨淋,锁身通常喷漆,锁勾通常是镀铬镍; (2)当锁芯转动不灵活时,可以向锁芯加入润滑剂,通常采用加入石墨粉的方法,石墨粉就是铅笔芯的粉末,所以本题答案为:注入铅...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com