
| 反应时间∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量∕g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
分析 高温条件下,碳酸钙分解生成氧化钙和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳质量可以计算碳酸钙质量,进一步可以计算该石灰石中含CaCO3的质量分数.
解答 解:(1)当石灰石完全反应后,生成CO2的质量为:80g-58g=22g,
故填:22.
(2)设该石灰石中碳酸钙质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,
100 44
x 22g
$\frac{100}{x}$=$\frac{44}{22g}$,
x=50g,
该石灰石中含CaCO3的质量分数为:$\frac{50g}{80g}$×100%=62.5%,
答:该石灰石中含CaCO3的质量分数为62.5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  向pH=3的溶液中不断加水 | |
| B. |  向锌粒中逐渐加入稀硫酸 | |
| C. | 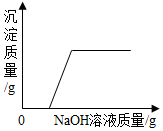 向稀硫酸和硫酸铜混合液中滴加氢氧化钠溶液 | |
| D. | 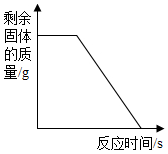 煅烧一定质量的石灰石 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20% | B. | 56% | C. | 80% | D. | 90% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 选项 | 物质 | 加入的试剂或操作 |
| A | NaCl 溶液(CaCl2) | 过量的碳酸钠溶液,过滤 |
| B | CaCO3(CaO) | 高温煅烧 |
| C | Cu(NO3)2 溶液(AgNO3) | 足量铜粉,过滤 |
| D | NaOH溶液(Ca(OH)2) | 适量的碳酸钠溶液,过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu+2AgCl═CuCl2+2Ag | B. | KOH+H2SO4═K2SO4+H2O | ||
| C. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | D. | CO2+Ca(OH)2═CaCO3↓+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫酸钾(K2SO4) | B. | 尿素【CO(NH2)2】 | ||
| C. | 磷酸二氢钙【Ca(H2PO4)2】 | D. | 磷酸二氢铵【(NH3)2H2PO4】 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com