


科目:初中化学 来源: 题型:
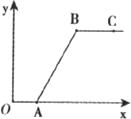 23、在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质).为了对废液进行处理,某同学做了如下实验:取废液缸上层清液40mL于烧杯中,逐滴滴入碳酸钠溶液至过量,滴入碳酸钠溶液的质量(x)与有关量的变化关系如图所示.
23、在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质).为了对废液进行处理,某同学做了如下实验:取废液缸上层清液40mL于烧杯中,逐滴滴入碳酸钠溶液至过量,滴入碳酸钠溶液的质量(x)与有关量的变化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 实验探究让化学更具魅力,请帮助完成下列实验探究
实验探究让化学更具魅力,请帮助完成下列实验探究| 白色粉末的成分 | 形 成 的 原 因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应: 化学方程式为: CO2+Ca(OH)2=CaCO3↓+H2O CO2+Ca(OH)2=CaCO3↓+H2O |
| 可能是 Ca(OH)2 Ca(OH)2 |
随着气温的升高,溶质的溶解度会 变小 变小 填变大或变小)或溶剂蒸发,石灰水中的溶质析出 |
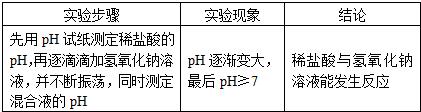
| 实 验 步 骤 | 可能观察到的现象 | 结 论 |
| 取上述试管中的上层清液,滴加1~2滴无色酚酞试液 | 溶液变红 | 白色粉末中含Ca(OH)2 白色粉末中含Ca(OH)2 |
| 往上述试管内残留的固体中加入稀盐酸 | 产生气泡 产生气泡 |
白色粉末中含有CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 某班同学在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质).为了对废液进行处理,某同学做了如下实验:取废液缸上层清液20.0g于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液直至过量,滴入碳酸钠溶液的质量与生成沉淀的质量的变化关系如图所示.
某班同学在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质).为了对废液进行处理,某同学做了如下实验:取废液缸上层清液20.0g于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液直至过量,滴入碳酸钠溶液的质量与生成沉淀的质量的变化关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com