
| 选项 | 物质 | 所选试剂及操作方法 |
| A | Cu(CuO) | 通入氧气并加热 |
| B | NaCl液(Na2CO3) | 加入适量氯化钙溶液充分反应后过滤 |
| C | CaO(CaCO3) | 加入适量稀盐酸溶解、过滤 |
| D | CO2(HCl) | 气体通过盛有足量氢氧化钠溶液洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Cu能与通入氧气并加热反应生成氧化铜,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、Na2CO3能与适量氯化钙溶液反应生成碳酸钙沉淀和氯化钠,充分反应后过滤,能除去杂质但引入了新的杂质,不符合除杂原则,故选项所采取的方法正确.
C、CaO和CaCO3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 智慧小复习系列答案
智慧小复习系列答案科目:初中化学 来源: 题型:解答题
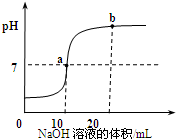 数字化装备正逐步进入各个校园.在盐酸和氢氧化钠反应的过程中,如图是利用数字化传感器得到的溶液pH变化图象.
数字化装备正逐步进入各个校园.在盐酸和氢氧化钠反应的过程中,如图是利用数字化传感器得到的溶液pH变化图象.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | LiMnO2为新型氧化物 | B. | LiMnO2为锂.锰.氧的合金 | ||
| C. | 该反应属于化合反应 | D. | 该反应中Mn元素的化合价没有变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
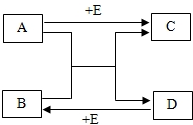 已知A、B、C、D、E均为初中化学常见的物质,他们之间的转化关系如图所示.部分生成物及反应条件已略去.
已知A、B、C、D、E均为初中化学常见的物质,他们之间的转化关系如图所示.部分生成物及反应条件已略去.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. | 气体燃烧,产生黄色火焰并伴有浓烈黑烟. | 电石与水反应产生的气体是乙炔(或C2H2) |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. | 固体溶解,无气泡放出. | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴酚酞. | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
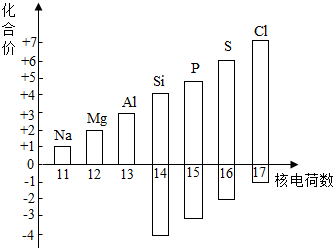 了解物质的组成和结构,有助于认识物质的性质.
了解物质的组成和结构,有助于认识物质的性质.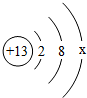 ,则最外层电子数x=3;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为Al3+.
,则最外层电子数x=3;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为Al3+.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 14g碳与32g氧气反应,根据质量守恒推出生成的二氧化碳的质量为46g | |
| B. | 聚乙烯燃烧生成二氧化碳和水,根据元素守恒推出聚乙烯由碳、氢、氧三种元素组成 | |
| C. | 50 mL 36%的盐酸用50mL水稀释,根据溶质守恒推出稀盐酸的溶质质量分数为18% | |
| D. | 水电解生成H2和O2的分子数比为2:1,根据原子守恒推出水分子中H、O原子数比为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②④ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com