
【题目】铁是目前使用最广泛的金属。请回答下列问题。
(1)身体一旦缺铁可能患有的疾病是__________。
(2)工业炼铁的主要设备是_________。工业上选用赤铁矿(主要成分Fe2O3)为原料炼铁的化学反应方程式为_________。
(3)不锈钢是铁、铬(Cr) ,镍(Ni)的合金,常用来制造医疗器械、餐具等。通过实验得知,铬和镍两种金属都能与稀硫酸反应生成氢气,分别得到硫酸铬(CrSO4)和硫酸镍(NiSO4)溶液。请写出铬(Cr)与稀硫酸反应的化学方程式_______________。
(4)铁生锈的主要过程为![]()
Ⅰ.写出转化①的化学方程式_________________。
Ⅱ.转化③生成![]() ,则x≤______________(x为整数)。
,则x≤______________(x为整数)。
【答案】缺铁性贫血 炼铁高炉 Fe2O3+3CO![]() 2Fe+3CO2 Cr+H2SO4=CrSO4+H2↑ 2Fe+2H2O+O2=2Fe(OH)2 3
2Fe+3CO2 Cr+H2SO4=CrSO4+H2↑ 2Fe+2H2O+O2=2Fe(OH)2 3
【解析】
(1)身体一旦缺铁可能患有的疾病是缺铁性贫血;
(2) 工业炼铁的主要设备是炼铁高炉,工业上选用赤铁矿(主要成分Fe2O3)为原料炼铁的原理是氧化铁和一氧化碳在高温条件下反应生成铁和二氧化碳,化学反应方程式为Fe2O3+3CO ![]() 2Fe+3CO2;
2Fe+3CO2;
(3)铬(Cr)与稀硫酸反应生成硫酸亚铬和氢气,化学方程式为Cr+ H2SO4 = Cr SO4 + H2↑;
(4)铁生锈的主要过程为![]()
Ⅰ.写出转化①的化学方程式2Fe+2H2O+ O2=![]() ;
;
Ⅱ.![]() 中铁和氢的原子个数比为1:3,据质量守恒定律可知反应前后原子的种类、个数不变,转化③生成
中铁和氢的原子个数比为1:3,据质量守恒定律可知反应前后原子的种类、个数不变,转化③生成![]() ,则x≤3。
,则x≤3。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:
【题目】某综合实践小组用溶质质量分数为10%的稀硫酸,对某造纸厂排放含NaOH的碱性废水进行检测。
(1)用溶质质量分数为98%、密度是1.84 g·mL-1的浓硫酸来配制100 g 10%的稀硫酸。配制的有关步骤依次为计算、____、稀释、转移装瓶、贴上标签。
(2)取含NaOH的碱性废水200 g,置于烧杯中,滴加2~3滴____。再向烧杯中边搅拌边滴加溶质质量分数为10%的稀硫酸39.2 g,反应恰好完全,此时溶液由红色刚好变为____色。计算碱性废水中NaOH的质量分数____(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是元素周期表中的一格,从中获取的信息正确的是( )

A. 该元素属于非金属元素
B. 该元素离子的核外有20个电子
C. 该元素原子的核内有20个质子
D. 该元素原子的质量为40.08g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学方法改造物质——“二氧化碳变汽油”。
二氧化碳是化石燃料燃烧的产物,汽油(主要成分为含有5个-11个碳原子的碳氢化合物)是全球用量最大的液体燃料.如果有人告诉你“二氧化碳能变成汽油”,你相信吗?近日,中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过如图示意的I、II、III三个环节,将二氧化碳成功转化为汽油.(图中a、b是两种起始反应物的分子结构模型,c、d是最终制得的汽油中所含物质的分子结构模型)
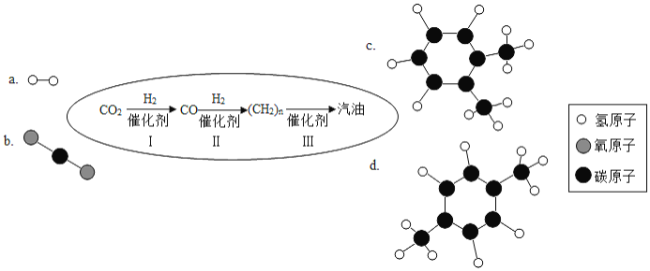
回答问题:
(1)催化剂能实现物质间的高效转化。下列有关催化剂的叙述正确的是__________ (填标号)。
A.催化剂可以改变化学反应速率
B.化学反应前后催化剂的质量不变
C.化学反应前后催化剂的化学性质发生改变
(2)在一定温度、压强及催化剂的条件下,环节I还生成了一种相对分子质量最小的氧化物,写出化学方程式:___________。
(3)观察c和d的分子结构模型,二者是否为相同物质? _______ (填“是”或“否”)。写出c的化学式:_______。
(4)“二氧化碳变汽油”的成果使我国成为此领域的领跑者。你认为该成果可解决的问题是__________、________ (答出两条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将金属镓做的勺子放入90℃的热水中,勺子很快就熔化;当水温降到26℃时,水中有凝 固的金属镓。己知镓在元素周期表中的信息和镓的一种粒子的结构示意图分别如图2、图3所示。下列说法错误的是

A. 金属镓的熔点高于26℃,低于90℃
B. 镓的相对原子质量是69.72
C. 镓原了核外有31个电子
D. 图3所表示粒子的化学符号是Ga
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】山药中含有“药用黄金”薯蓣皂素(化学式为C27H42O3)。下列有关薯蓣皂素的说法正确的是
A. 薯蓣皂素属于氧化物
B. 207g薯蓣皂素中含有8g的氧元素
C. 薯蓣皂素中碳、氢元素的质量比为54:7
D. 薯蓣皂素是由27个碳原子、42个氢原子和3个氧原子构成的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一根部分氧化的镁条(只含氧化镁一种杂质),测得其中含镁元素的质量分数为80%,取此部分氧化的镁条3.0g与100g的稀硫酸恰好完全反应。则反应所使用的稀硫酸溶液中硫酸的质量分数为(已知:MgO+H2SO4=MgSO4+H2O)
A. 19.6% B. 4.9% C. 9.8% D. 无法确定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答问题。
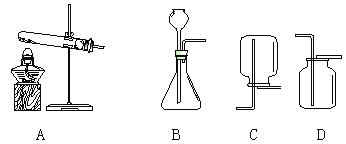
(1)实验室制二氧化碳可选用的发生装置是(填序号)_______。
(2)能用D装置收集CO2的原因是_________。
(3)实验室用高锰酸钾制氧气时,反应的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化氢在生产生活中有着广泛的应用。化学实验小组对过氧化氢的某些性质进行了研究。
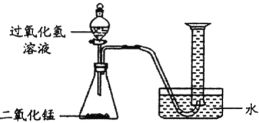
Ⅰ.不稳定性
(1)如图所示进行实验(还测量收集的氧气体积),过氧化氢分解的化学方程式为_________________。
(2)能用排水法收集氧气的原因是 _________________________。
(3)已知:常温常压下,氧气的密度为1. 33 g·L–1。实验小组称量了10 g溶质质量分数为 6%的过氧化氢溶液进行实验,如果将该过氧化氢溶液一次性全部放入锥形瓶中,则选择规格为________mL(选填“50”、“200”或“250"”)的量筒收集氧气较为合适。
(4)实验小组同学还探究了温度对过氧化氢分解速率的影响,相关实验数据如下表:
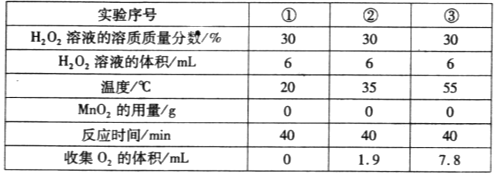
由此得出的结论是_________________________。
Ⅱ.腐蚀性
(查阅资料)H2O2溶液有一定的腐蚀性。
(进行实验)将铜片分别浸泡在以下3种溶液中进行实验,实验现象如下表:
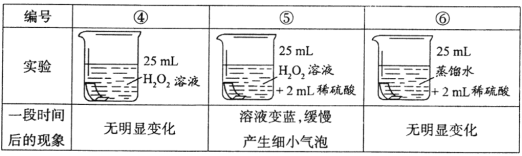
(解释与结论)
(5)实验④的作用是________________。
(6)实验⑤中铜片被腐蚀的反应为Cu + H2O2+ H2SO4=CuSO4+□________,请补全该反应的化学方程式。
(反思交流)
(7)小红同学提出,实验⑤中除发生(6)所给的反应外,还发生了另一个反应导致有细小的气泡产生,该反应的反应物是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com