【答案】
分析:(1)利用铁活动性比铜强,可选取可溶性铜盐与铁粉反应而除去混在铜粉中的铁粉;
(2)根据复分解反应的交换成分的特点,可选取一种可溶性碱与碳酸钠反应生成氢氧化钠和一种沉淀而除去杂质碳酸钠;
(3)根据复分解反应交换成分的特点,可选取一种可溶性盐与氯化钙反应,把氯化钙转变成氯化钠同时生成钙盐的沉淀而除去杂质氯化钙;
(4)根据复分解反应交换成分的特点,可选取一种可溶性盐与硫酸钾反应,把硫酸钾转变为氯化钾同时生成一种硫酸盐的沉淀而除去硫酸钾;
(5)由于氧化钙遇水会发生反应,因此只能利用碳酸钙在高温下分解的性质,采取继续锻烧的方法除去混在氧化钙中的碳酸钙杂质,而不能使用其它溶液.
解答:解:(1)将混有铁粉杂质的铜粉放入硫酸铜溶液,铁与硫酸铜反应生成硫酸亚铁和铜,而除去混合粉末中的铁粉,反应的化学方程式为Fe+CuSO
4═Cu+FeSO
4;
(2)向混有碳酸钠杂质的氢氧化钠中加入适量的氢氧化钙溶液,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,充分反应后过滤即可达到除去混合物中的碳酸钠的目的,反应的化学方程式为Na
2CO
3+Ca(OH)
2═CaCO
3↓+2NaOH;
(3)向混有少量杂质氯化钙的氯化钠中加入适量的碳酸钠溶液,使氯化钙与碳酸钠反应生成氯化钠和碳酸钙沉淀,充分反应后过滤,可达到除去混在氯化钠中氯化钙杂质的目的,反应的化学方程式为CaCl
2+Na
2CO
3═CaCO
3↓+2NaCl;
(4)向混有少量硫酸钾杂质的氯化钾中加入适量的氯化钡溶液,使硫酸钾与氯化钡反应生成硫酸钡沉淀和氯化钾,充分反应后过滤,可达到除去混在氯化钾中少量的硫酸钾杂质的目的,反应的化学方程式为K
2SO
4+BaCl
2═BaSO
4↓+2KCl;
(5)将混有少量碳酸钙杂质的氧化钙继续高温锻烧,可使碳酸钙分解为氧化钙和二氧化碳,而除去混合物中的碳酸钙,反应的化学方程式为CaCO
3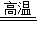
CaO+CO
2↑.
故答案为:
(1)Fe+CuSO
4═Cu+FeSO
4;
(2)Na
2CO
3+Ca(OH)
2═CaCO
3↓+2NaOH;
(3)CaCl
2+Na
2CO
3═CaCO
3↓+2NaCl;
(4)K
2SO
4+BaCl
2═BaSO
4↓+2KCl;
(5)CaCO
3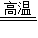
CaO+CO
2↑.
点评:在采取化学的方法除去混合物中的杂质时,所选用的试剂或方法应只能将混合物中杂质反应掉而不能使其主要成分发生反应,方能达到除去杂质的目的.

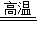 CaO+CO2↑.
CaO+CO2↑.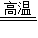 CaO+CO2↑.
CaO+CO2↑.
