
����Ŀ��dzdzͬѧ���˱Ƚ����ص�θ�ף�����Ϻ������У��������������ѧ�й�ϵ������һ�����������ɽ��ɣ�
һ��Ϊ����ϣ�ҽ���������˱�����Ӱ�������͡���ҽ�õ�__________���ѧʽ���������Ա����ж�����������Ϊ0.8g�����Dz�����ˮ��̼�ᱵ�Խ����ӣ�Ҳ��ʹ���ж������û�ѧ����ʽ����ԭ��__________����С�����̼�ᱵ�����������������ڼ��Ƚⶾ����__________��
A��ţ�� B��ʳ��ˮ C������þ��Һ D�������� E������ͭ��Һ
����ҽ�����dzdz��θ�����������θ����������Һ���ƣ����ڷ�����ҩ������ơ�������Ҫ�ɷֱȽ��ʺ��������ҩ����__________��
A��˹����[Al(OH)3 ] B��Stomachease��Mg(OH)2] C�����������ң�NaHCO3]
һЩ����ʳ��Ľ���pH���£�dzdz�ո�ʱ���ʳ��__________��
A��ţ�̣�6.3-6.6�� B�������ࣨ6.8-8.0�� C������֭��4.0-4.4�� D��������6.0-7.0��
����dzdz��Һʱʹ���ˡ�һ������Һ���������������Լ��½����������Һ�ﵽ30�����ң����ܳ���4Сʱ���ϡ���Һ������Ϊʲô�ܷ��ȣ��������Ҫ�ɷ�����ʲô��

���ϵ�ͬѧ������ʦ�����½�����ʵ��̽����
������İ�װ��������һ�Ѻ�ɫ�����ĩ��
�����۽�����
��1����������ͼ˵���飬�������ͼ��ʵ�鷽������֤����ɫ��ĩ�Ƿ���̼�ۡ����ַ����Ƿ���У�__________��������__________��̼�۲����������γ�����С��ԭ��أ���������������ˮ��ʹ��Ӧ����ؽ��С�

��2�����ݳ��л�ѧ֪ʶ����Ϊ����ԭ���ǡ����ۻ����������ų������������Ȼ��Ƶ�������__________���ڴ˱仯��__________��ת��Ϊ__________�ܡ�
��3�����һ��ʵ����֤��ɫ��ĩ�к����Ȼ���
���� | ���� | ���� |
ȡ������ɫ��ĩ��ˮ�ܽ����ˣ�����Һ�����Թ��У��μ�����__________��Һ��__________�����������ƣ� | _________�� | �����Ȼ��� |
��4��ͬѧ��Ϊ�����������ַ���װ�ã����ⶨ��ѻ�����е�����̼�����ȡ�����ȡ��������ʵ��ʣ�µĺ�ɫ��ĩ����������ʵ�顣
���������ϡ���
��2Fe(OH)3![]() Fe2O3+3H2O
Fe2O3+3H2O
��Fe+2FeCl3=3FeCl2
����HCl��FeCl3�Ļ����Һ��Fe����FeCl3��Ӧ
��ʵ���¼����

��ʵ����ۡ���
��д��dz��ɫ��Һ��Ϊ���ɫ�����Ļ�ѧ����ʽ__________������ʵ��ⶨ����Һ�����������ۺ�̼�۵�������Ϊ__________�������軯Ϊ��������ȣ�����Ѿ����������ĺ�ɫ��ĩ��ʣ�����������Ϊ__________g��
���𰸡� BaSO4 BaCO3+2HCl=BaCl2+H2O+CO2 �� BE AB B ������ �ƾ�ȼ��Ҳ�����������̼ �ӿ�������ʴ ��ѧ �� ������ ϡ���� ���ɰ�ɫ�����ҳ������ܽ� 4FeCl2 +4 NaOH +O2 +2H2O == 2Fe(OH)3��+ 4NaCl 7.28:1.9 6.16
��������һ�������͡���ҽ�õ����ᱵ����ѧʽΪBaSO4 ��̼�ᱵ��ϡ���ᷴӦ�����Ȼ�����ˮ�Ͷ�����̼���÷�Ӧ�Ļ�ѧ����ʽΪ��BaCO3+2HCl=BaCl2+H2O+CO2���������Ե��ؽ����Σ��ܵ�����ؽ������ӣ������ƻ������ʵĽṹ�����ú��зḻ�����ʵ�ʳƷ����ת��Ϊ��������ij������ɷ�ֹ���屾���ĵ����ʱ��ƻ����нⶾ���ã�ţ�̡������庬�зḻ�ĵ����ʣ�����þ��Һ�������Ȼ�����Ӧ�������ᱵ�������Ȼ�þ���Ȼ������Ȼ�������Ӧ������ͭ��Һ�����ж���
��������̼��������θ�ᣨ��Ҫ�ɷ�Ϊ���ᣩ��Ӧ����������Ķ�����̼���壬������θ�����ˣ����Կڷ�������������������þ��ҩ���к�θ�dzdzθ����࣬���Է��ü��Ե�ʳƷ��������pHΪ6.8-8.0������Ҫ����
������1��̼ȼ�������ɶ�����̼�����ھƾ�ȼ��Ҳ�����������̼����֤�����ɵĶ�����̼����̼��ȼ�գ�
��2���Ȼ������Σ��ܼӿ�������ʴ����Ӧ���е�Խ�죬��ʱ���ڷų�������Խ�࣬�˹����л�ѧ��ת��Ϊ���ܣ�
��3�����һ��ʵ����֤�ڷ��к����Ȼ��ƣ���֤�������ӵĴ��ڣ�����ʹ�ü�����������Һ�����μ�ϡ���ᣬ���۲쵽��ɫ�����������ҳ���������ϡ��������������Ȼ��ơ�
��4��dz��ɫ��Һ���Ȼ����������ɫ����Ϊ�����������Ȼ������������Լ�����������ˮ��Ӧ����������������ѧ����ʽΪ4FeCl2 +4 NaOH +O2 +2H2O=2Fe(OH)3��+ 4NaCl��
ʵ���к�ɫ��������̼�ۣ�����Ϊ1.9g����Ʒ�е���ת��Ϊ��������������ɫ��ĩ���е�����������������Ϊ10.4g��![]() =7.28g��������Һ�����������ۺ�̼�۵�������Ϊ7.28:1.9��
=7.28g��������Һ�����������ۺ�̼�۵�������Ϊ7.28:1.9��
��Ʒ�е����������ᷴӦ�����Ȼ�������������
����Ʒ�е�����������Ϊx
Fe+2HCl�TFeCl2+H2��
56 2
x 0.2g
![]()
x=5.6g��
��HCl��FeCl3�Ļ����Һ��Fe����FeCl3��Ӧ����Fe + 2FeCl3 = 3FeCl2��֪��ʣ����Ԫ������![]() ���������ʣ�������FeCl3��Ӧ��������Ϊ��7.28g-5.6g����
���������ʣ�������FeCl3��Ӧ��������Ϊ��7.28g-5.6g����![]() =0.56g����������Ѿ����������ĺ�ɫ��ĩ��ʣ�����������Ϊ5.6g+0.56g=6.16g��
=0.56g����������Ѿ����������ĺ�ɫ��ĩ��ʣ�����������Ϊ5.6g+0.56g=6.16g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��A��B��C���ֹ������ʵ��ܽ�����ߣ���ش�
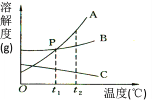
��1�����������У��ܽ�����¶�Ӱ���С����_____��
��2��t1��ʱ���߽���P��ʾ______��
��3��t2��ʱA���ʵIJ�������Һ��ɱ�����Һ�ķ�����______��
��4��A�����л�������B����ʱ���ɲ���_____________�ķ����õ��ϴ�����A���ʡ�
��5��t1��ʱA��B��C�������ʵı�����Һͬʱ���µ�t2������ʱ��Һ���������������Ĵ�С��ϵ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ϊͬ�����������
A. ���ͺ��� B. ������Һ�� C. ���ɱ� D. ˮ��˫��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������ƿ����δ����ǩ��ֻ֪�����Ƿֱ���̼�����(NH4HCO3)���Ȼ��(NH4Cl)������[CO(NH2)2]�е�һ�֡�Ϊ�������ֻ��ʣ�ijͬѧ�ֱ�ȡ������Ʒ���ΪA��B��C������������ʵ��(�˴���ͷ��ʾ�ó�ʵ�����)��

��������ʵ��ش�
(1)д�����ֻ��ʵ����ƣ�
A ��B ��C ��
(2)���ʵ������B��C������Ʒû����ȡ����ʵ���� (��С����ޡ�)Ӱ�졣
(3)��������Ҫ����B��C������Ʒ�� (��ܡ����ܡ�)��ȡ����ζ�ķ�����
(4)��ʵ��Ͳ������Ͽ�֪��������ʩ���̬����ʱ���������������ʣ���ʹ�̬����ת��Ϊ�����������������������ˮ���ã������γɡ����ꡱ�������ꡱ�м�Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���;�����ʶ�Ӧ��ϵ����������
A. ʯī����ص缫�������� B. һ����̼ұ����������ȼ��
C. ���ʯ�и����Ӳ�ȴ� D. ����̿����ζ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽס��ҡ��� ���ֹ������ʣ������ᾧˮ�����ܽ�����ߣ� ����˵����ȷ���ǣ� ��

A. t1��ʱ�ҡ����������ʵ���Һ�����ʵ���������һ�����
B. ��t1��ʱ�ס��ҡ����������ʵı�����Һ���µ�t3��ʱ�����õ���Һ�����������������Ǽ�
C. ���л�����������ʱ��Ӧ���������ᾧ�ķ����ᴿ��
D. t3��ʱ�����������ļס��ҡ�������������ɱ�����Һ�����ˮ�����������DZ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������뷴˼��ѧϰ��ѧ����Ҫ���ڡ����й�����ȫ��ȷ����
A����������; | B��ȼ�������� | C�����ʵļ��� | D�����������ӹ��� |
��������ȼ�ԡ���ȼ�� ������ѧ���ʲ����á����������������ܶȱȿ���С����ѧ�����ȶ�����̽������ | ���ڿ�����ȼ�ա���������ɫ��������˿ȼ�ա���������������ȼ�ա������������� | ��ˮ��Ӳˮ������ˮ O2��CO2��N2��ȼ�ŵ�ľ����H2O��H2O2������������� | ����ͭ����ͭԭ�ӹ������������������ӹ������Ȼ��ơ��������Ӻ������ӹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�У��������ʻ�ѧ���ʵ���
A. ��ͨ������������Ʒ B. ������̼��ʹ����ʯ��ˮ�����
C. ���ʯӲ�ȴ� D. ʢ��ˮ��ֲ���͵��Թ��õ���״����Һ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com