
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
分析 (1)第一次和第二次所取的固体质量不等,但是所取氯化钙溶液的质量相等,但是生成的沉淀的质量相等,所以可以判断第一次所取固体有剩余,即5g固样品反应后能生成沉淀的质量为4g,第2次和第3次所取的固体样品相等,但是所取的氯化钙溶液的质量不等,但是生成的沉淀的质量相等,所以可以判断第3次所取的氯化钙溶液有剩余,即说明50g氯化钙溶液反应后只能得到4g沉淀,综上分析可以知道第二次是所给的物质恰好完全反应,所以可以根据第2次反应的数据进行解答;根据生成沉淀的质量可以计算出碳酸钠、氯化钙的质量;
(2)根据氯化钙的质量计算出氯化钙溶液的质量分数;
(3)根据(1)中所求碳酸钠的质量可以计算出杂质中氯化钠的质量及氯化钠的质量分数.
解答 解:(1)由题意分析李明的实验数据可知,第一次和第二次所取的固体质量不等,但是所取氯化钙溶液的质量相等,但是生成的沉淀的质量相等,所以可以判断第一次所取固体有剩余,即5g固样品反应后能生成沉淀的质量为4g,第2次和第3次所取的固体样品相等,但是所取的氯化钙溶液的质量不等,但是生成的沉淀的质量相等,所以可以判断第3次所取的氯化钙溶液有剩余,即说明50g氯化钙溶液反应后只能得到4g沉淀,综上分析可以知道第二次是所给的物质恰好完全反应.
设碳酸钠的质量为x,参加反应的氯化钙质量为y
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111 100
x y 4g
$\frac{106}{x}=\frac{111}{y}=\frac{100}{4g}$ 解得:x=4.24g,y=4.44 g
(2)加入的氯化钙溶液的溶质质量分数为:$\frac{4.44g}{50g}$×100%=8.88%;
(3)碳酸钠样品中杂质氯化钠的质量:5g-4.24g=0.76g;
碳酸钠样品中杂质氯化钠的质量分数是 $\frac{0.76g}{5g}$×100%=15.2%;
答:(1)5g碳酸钠样品中碳酸钠的质量是4.24g;
(2)加入氯化钙溶液的溶质质量分数是8.88%;
(3)碳酸钠样品中杂质氯化钠的质量分数是15.2%
点评 本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
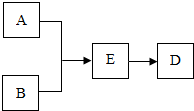 A、B、D、E是初中化学常见物质,分别由C、H、O、S、Ca、Fe等七种元素中的一种或几种组成,四种物质的转化关系如图所示,其中D在常温下为一种生命活动不可或缺的无色液体.其中“→”表示转化关系.
A、B、D、E是初中化学常见物质,分别由C、H、O、S、Ca、Fe等七种元素中的一种或几种组成,四种物质的转化关系如图所示,其中D在常温下为一种生命活动不可或缺的无色液体.其中“→”表示转化关系.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
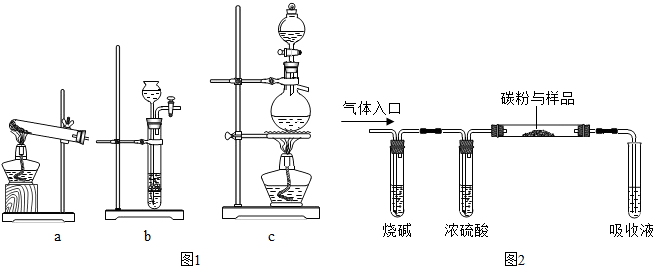
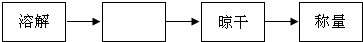
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石墨烯的化学式为C | B. | 石墨烯的硬度小于金刚石 | ||
| C. | 石墨烯属于化合物 | D. | 石墨烯不能导电 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
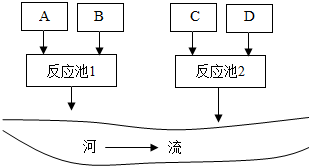 某化学试剂厂A,B,C,D四个车间排放的废水中,分别含有氢氧化钠、硫酸铜、碳酸钠、硫酸中的一种,在不加其他试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流.如图所示:
某化学试剂厂A,B,C,D四个车间排放的废水中,分别含有氢氧化钠、硫酸铜、碳酸钠、硫酸中的一种,在不加其他试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流.如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一块金属很难被压缩,说明原子之间没有间隔 | |
| B. | 湿衣服晾在太阳下干的快,说明分子运动速率与温度有关 | |
| C. | 将二氧化碳气体制成干冰,体积变小是由于分子体积变小 | |
| D. | 分离液态空气制氧气说明分子可以再分 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com