
分析 (1)化合物化学式的读法:一般是从右向左读,读作“某化某”.
(2)根据位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此进行分析解答.
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)KI右向左读,读作碘化钾.
(2)位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,铜的金属活动性比银强,能与硝酸银溶液反应生成硝酸铜和银.
(3)①NaOH溶液与HCl溶液混合生成氯化钠和水,反应的化学方程式为:HCl+NaOH=NaCl+H2O.
②KI溶液与AgNO3溶液混合生成碘化银沉淀和硝酸钾,反应的化学方程式为:KI+AgNO3=AgI↓+KNO3.
故答案为:(1)碘化钾;(2)AgNO3;(3)①HCl+NaOH=NaCl+H2O;(2分) ②KI+AgNO3=AgI↓+KNO3.
点评 本题难度不大,掌握盐的化学性质、化合物化学式的读法、金属的化学性质并能灵活运用是正确解答本题的关键.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:初中化学 来源: 题型:实验探究题
| 实验编号 | 一、探究人体呼出气体中二氧化碳含量比空气中的高 | 二、探究影响品红扩散快慢的因素 | 三、铁钉锈蚀条件的探究 |
| 实验设计 | 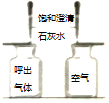 | 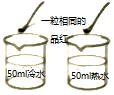 | 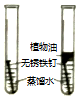 |
| 实验分析 | 本实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制滴入澄清石灰水的体积相同. | 发现两杯水都变红,且整杯热水变红时间比冷水要短.由此说明:①分子在不断运动;②影响分子运动快慢的因素有温度. | 一周后,左边试管中铁钉生锈,右边试管中铁钉无明显变红,上述实验不能(填“能”或“不能”)得出铁钉生锈的条件 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将地沟油转化为航空油,变废为宝 | |
| B. | 使用新型的可降解塑料,减少白色污染 | |
| C. | 改进汽车尾气净化技术,减少有害气体排放 | |
| D. | 加高化工厂的烟囱排放废气,防止形成酸雨 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
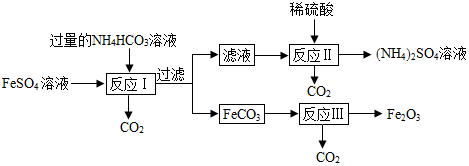
| A. | 反应Ⅰ需控制温度在35℃以下,原因可能是因为NH4H CO3受热易分解 | |
| B. | 滤液中的溶质只有( NH4)2 SO4 | |
| C. | 在空气中煅烧23.2g的FeCO3,得到Fe2O3和FeO的混合物15.2g.则生成Fe2O38.0g | |
| D. | 在空气中充分煅烧FeCO3,若煅烧时间越多,则最终所得固体的质量越小 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 借助酚酞试液可完成稀盐酸、NaCl溶液、NaOH溶液、K2CO3(草木灰的主要成分)溶液间的鉴别 | |
| B. | 把金属钠放入硫酸铜溶液中,会发生置换反应,得到红色固体生成 | |
| C. | 除去FeCl2溶液中的CuCl2的方法是加入过量的铁粉,再过滤 | |
| D. | 在不用指示剂的情况下,选用CaCO3粉末将含有盐酸的CaCl2溶液的pH等于7 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
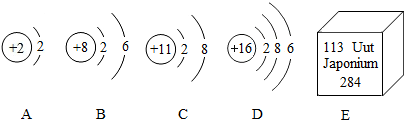
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
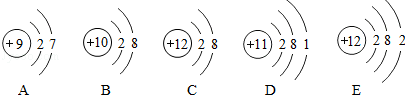
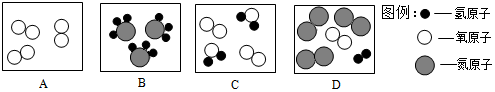
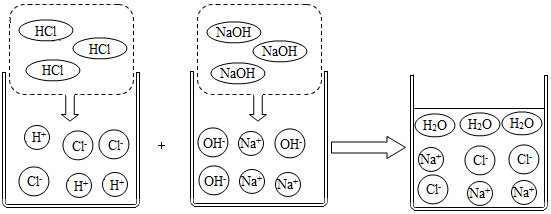
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com