
| A. | 扑灭森林火灾时设置隔离带 | |
| B. | 加油站,面粉加工厂等场所要严禁烟火 | |
| C. | 烧煤取暖时注意开窗通风 | |
| D. | 为了美观用砂纸将铝制品表面打磨光亮 |
分析 A、根据燃烧的条件和灭火的原理进行分析判断;
B、面粉厂的空气中常混有可燃性的微粒,空间有限,遇明火容易引起爆炸;
C、煤不完全燃烧会生成一氧化碳;
D、铝与空气中氧气反应生成一层致密的氧化铝薄膜,可阻止里面的铝进一步反应;
解答 解:A、扑灭森林火灾时,设置防火隔离带的目的是使可燃物与燃烧物隔离;故选项说法正确;
B、面粉属于可燃性粉尘,与氧气混合达到一定程度时遇明火会发生爆炸,所以面粉加工厂、加油站要严禁烟火;故选项说法正确;
C、煤不完全燃烧会生成一氧化碳,一氧化碳能和血红蛋白结合使人缺氧,故烧煤取暖时要注意通风良好,故选项说法正确;
D、铝与空气中氧气反应生成一层致密的氧化铝薄膜,可阻止里面的铝进一步反应,用砂纸打磨会破坏氧化铝薄膜,缩短铝制品的使用寿命,故选项说法错误.
故选D.
点评 本题难度不大,考查同学们结合生活实际灵活运用所学燃烧的条件、灭火的原理、爆炸等知识进行解题的能力.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:初中化学 来源: 题型:多选题
| A. | 磷在空气中燃烧产生浓厚的白雾 | |
| B. | 硫在空气中燃烧产生蓝紫色火焰 | |
| C. | 点燃一氧化碳时,火焰呈蓝色,产物能使澄清石灰水变浑浊 | |
| D. | 往水中加入少量高锰酸钾,液体由无色变成红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 称量时,必须将氢氧化钠固体放在玻璃器皿中称量 | |
| B. | 称量氢氧化钠固体时应该将砝码放在左盘,药品放在右盘 | |
| C. | 实验中要用到的玻璃仪器只有烧杯和玻璃棒 | |
| D. | 实验中量取水时,需要选择规格为50毫升的量筒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
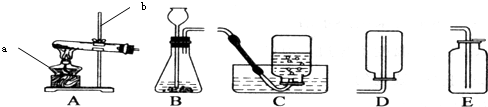
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 如图烧杯内壁出现水雾,说明甲烷中含有碳、氢两种元素 | |
| B. | 如图蜡烛自下而上熄灭,说明二氧化碳密度比空气大,不支持燃烧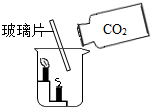 | |
| C. | 如图所示实验既说明电解水生成氢气和氧气,又说明水是由氢气和氧气组成的 | |
| D. | 如图铜片上的白磷燃烧而红磷不燃烧,说明红磷不是可燃物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com