
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 氢氧化钠 | D. | 氯化钠 |
分析 有些药品长期露置在空气中,会发生质量的变化(有的增加有的减少)或者变质,不同的物质由于其性质的不同暴露在空气中变化不同,像生石灰(氧化钙)、烧碱(氢氧化钠)、浓硫酸、铁等露置在空气中由于吸水或氧气反应导致质量增加;像浓氨水、浓盐酸、浓硝酸等由于挥发性其质量会减少.
解答 解:A、浓硫酸具有吸水性,能吸收空气中水蒸气,溶液质量增加,故此选项正确.
B、浓盐酸具有挥发性,挥发出氯化氢气体,溶质质量减少,溶液质量也减少,故此选项错误.
C、氢氧化钠固体在空气中会潮解并与二氧化碳反应,质量会增加,故此选项正确.
D、氯化钠固体在空气中无任何变化发生,质量不会变化,故此选项错误.
故选AC.
点评 此题考查常见的物质在露置空气中,自身质量的变化情况,由该题我们也联想到在化学实验室一些药品的保存一定要注意正确保存,否则会发生变化或者变质,带来不便.


科目:初中化学 来源: 题型:选择题
| A. | 用湿润的PH试纸测得某地酸雨的pH值为4.6 | |
| B. | 用通过灼热CuO粉末的方法除去CO2中的少量CO | |
| C. | 从MnO2与KCl的混合物中分离出KCl的方法是溶解、过滤、蒸发、结晶 | |
| D. | 只用一种试剂能鉴别出NaCl、NaOH、NH4NO3三种固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 常温下化学性质活泼 | B. | 具有吸附性 | ||
| C. | 在一定条件下可还原氧化铜 | D. | 在氧气中完全燃烧的产物是CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的量筒中 | |
| B. | 酒精灯使用完毕,用灯帽盖灭 | |
| C. | 用滴管滴加液体时,将滴管伸入试管中 | |
| D. | 不慎将硫酸洒在皮肤上,用氢氧化钠溶液中和 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  过滤 | B. | 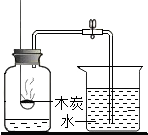 测定空气中氧气含量 | ||
| C. | 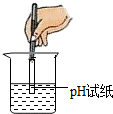 测定溶液的pH | D. | 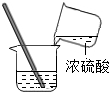 稀释浓硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 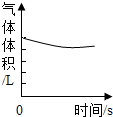 红磷在密闭的空气中燃烧 | B. | 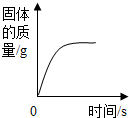 铁丝在充足的氧气中燃烧 | ||
| C. | 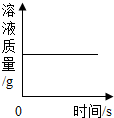 一定量稀硫酸中加入锌粒 | D. | 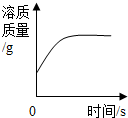 向某饱和碳酸钠溶液中加入碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 预期的实验现象 | 实验结论 |
| ①取一小块钟乳石于试管中,向试管中加稀盐酸观察现象. ②将产生的气体通入澄清的石灰水,观察现象. | 有气泡生成 有白色沉淀生成 | 钟乳石的主要成分是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com