

分析 (1)根据元素周期表中同一周期的规定来分析;
(2)根据最外层电子数大于4的都易得电子,并且电子数越大越易得以及化合物的化学式写法进行分析;
(3)每一周期元素原子的原子层相同,最外层电子依次增加;
(4)根据表中信息分析解答.
解答 解:(1)第二周期的3-10号元素原子的电子层数相同,第三周期的11-18号元素原子的电子层数也相同,因此得出规律每一周期元素原子的电子层数相同;故答案为:核外电子层数;
(2)9号元素最外层电子数为7,都易得到电子而达到稳定结构,属于非金属;与17号氯元素的化学性质相似;答案:得到;非金属;17号氯元素;
(3)每一周期元素原子的原子层相同,最外层电子从左至右依次增加;答案:从左至右依次增加;
(4)根据图2信息可知钙元素的相对原子质量是40.08;氟元素的质子数为9.答案:40.08;9.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、了解原子结构示意图的意义进行分析解题的能力.


科目:初中化学 来源: 题型:解答题
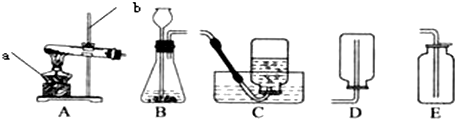
 小林同学设计如图所示的装置制取氧气
小林同学设计如图所示的装置制取氧气查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子能保持物质的化学性质而原子不能 | |
| B. | 分子间有间隙而原子间没有 | |
| C. | 化学变化中分子可以再分而原子不能再分 | |
| D. | 分子能构成物质而原子不能 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com