
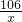 =
=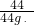 x=10.6g
x=10.6g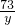 =
=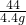 y=7.3g
y=7.3g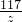 =
=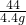 z=11.7g
z=11.7g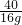 =
=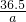 a=14.6g
a=14.6g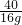 =
=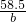 b=23.4g
b=23.4g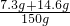 ��100%=14.6%
��100%=14.6%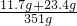 ��100%=10%
��100%=10%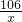 =
=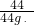 x=10.6g
x=10.6g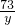 =
=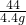 y=7.3g
y=7.3g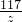 =
=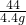 z=11.7g
z=11.7g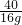 =
=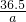 a=14.6g
a=14.6g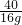 =
=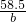 b=23.4g
b=23.4g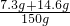 ��100%=14.6%
��100%=14.6%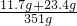 ��100%=10%
��100%=10%

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013����б�ҵ��ѧ���ԣ�������̶������ѧ�������棩 ���ͣ�̽����
ijʵ��С��Ϊ����¶���ڿ����е�NaOH�����Ƿ���ʲ�ȷ������ɣ���չ��һ��̽�����
�������뽻����
��1��NaOH��������е��� �����ѧʽ��������Ӧ����Na2CO3��
��2��Na2CO3��ˮ��Һ�ʼ��ԣ�
���������ϡ�
��3��NaOH�ڿ����в���ת����NaHCO3��
��4��CaCl2��NaCl��ˮ��Һ�������ԣ�
��������衿����һ������ȫ��ΪNaOH��
����һ������ȫ��Ϊ�� ����
����һ������ΪNaOH��Na2CO3�Ļ���
��ʵ��̽�����������������ˮ�����Һ�����������ַ�������ʵ�飺
����һ���ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ����pH�� �������������������=������˵������һ��������
��������ȡ����Һ�����������м�������CaCl2��Һ���а�ɫ�������������������ٲ��������ˣ�������Һ�е����̪��Һ����Һ����� ��ɫ��˵��������������
���������ܽ�����ԣ�����һ�Ľ����� �������ȷ���������������� ����
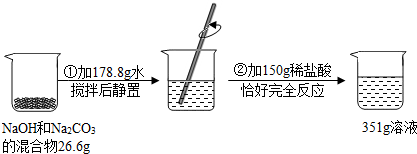
��̽������չ��Ϊ��һ��ȷ��ԭ�������ɣ���ʵ��С���ͬѧ��ȡ26.6g������壬����ͼ��ʾ����ʵ�飨����ڲ���������ȫ���ݳ����������ͼ���ṩ�����ݼ��㣺
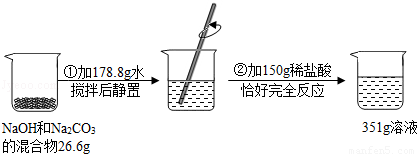
��5��26.6g����������Na2CO3��������
��6������ϡ���������ʵ�����������
��7��ʵ����������351g��Һ�����ʵ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013����б�ҵ��ѧ���ԣ�������̶������ѧ�������棩 ���ͣ�̽����
ijʵ��С��Ϊ����¶���ڿ����е�NaOH�����Ƿ���ʲ�ȷ������ɣ���չ��һ��̽�����
�������뽻����
��1��NaOH��������е��� �����ѧʽ��������Ӧ����Na2CO3��
��2��Na2CO3��ˮ��Һ�ʼ��ԣ�
���������ϡ�
��3��NaOH�ڿ����в���ת����NaHCO3��
��4��CaCl2��NaCl��ˮ��Һ�������ԣ�
��������衿����һ������ȫ��ΪNaOH��
����һ������ȫ��Ϊ�� ����
����һ������ΪNaOH��Na2CO3�Ļ���
��ʵ��̽�����������������ˮ�����Һ�����������ַ�������ʵ�飺
����һ���ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ����pH�� �������������������=������˵������һ��������
��������ȡ����Һ�����������м�������CaCl2��Һ���а�ɫ�������������������ٲ��������ˣ�������Һ�е����̪��Һ����Һ����� ��ɫ��˵��������������
���������ܽ�����ԣ�����һ�Ľ����� �������ȷ���������������� ����
��̽������չ��Ϊ��һ��ȷ��ԭ�������ɣ���ʵ��С���ͬѧ��ȡ26.6g������壬����ͼ��ʾ����ʵ�飨����ڲ���������ȫ���ݳ����������ͼ���ṩ�����ݼ��㣺
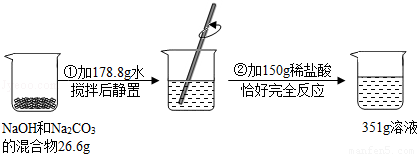
��5��26.6g����������Na2CO3��������
��6������ϡ���������ʵ�����������
��7��ʵ����������351g��Һ�����ʵ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�����ʡ��̶���п���ѧ�Ծ��������棩 ���ͣ������
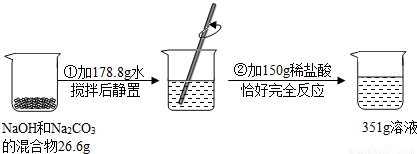
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com