
【题目】某兴趣小组同学用大理石和盐酸反应制取二氧化碳,将制得的气体通入澄清石灰水,观察到石灰水未变浑浊,他们对此现象产生了好奇。请你与他们一同探究:
(提出问题)为什么石灰水未浑浊?
(猜想假设)猜想①:石灰水已变质;
猜想②:制得的气体中无二氧化碳:
猜想③:_____。
(实验验证)(1)同学们为验证假设是否成立。他们将适量的原试剂瓶中的澄清石灰水倒入小试管中,然后_____(填写实验操作过程),他们根据实验现象确认了石灰水未变质。他们接着探究,通过实验又否定了猜想②。
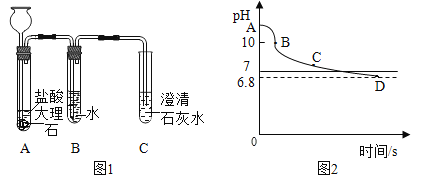
(2)同学们继续设计了如图1实验来探究猜想③:
①如图1,加入B装置后,C中澄清石灰水变浑浊。同学们通过实验确定了澄清石灰水未变浑浊的原因是二氧化碳中含有氯化氢气体,故猜想③正确。请用化学反应方程式解释将制得的气体通入澄清石灰水后,石灰水不变浑浊的原因_____。
②B装置的作用是_____,实验后向B中滴入石蕊溶液,可看到的现象是_____,写出B中主要溶质的化学式:_____。
(3)小组同学pH传感器测得纯净二氧化碳通入澄清石灰水中pH的变化曲线。如图2所示,已知BC段反应生成的是可溶于水的碳酸氢钙的过程。请你回答:①A点溶液的pH约为_____,AB段pH下降较快的原因是_____(用化学方程式表示)
②D点溶液中的溶质化学式为:_____。
【答案】可能是二氧化碳中的氯化氢气体导致石灰水不浑浊 用导管向澄清石灰水中吹气(或滴加酚酞溶液变红等合理答案也可) 2HCl+Ca(OH)2=CaCl2+2H2O 吸收氯化氢气体 紫色石蕊溶液变红 HCl(填HCl、H2CO3或HCl、H2CO3、CO2,也给分,但是没有HCl不给分) 填12或14 CO2+Ca(OH)2=CaCO3↓+H2O Ca(HCO3)2、H2CO3;或填H2CO3给分,但是只填Ca(HCO3) 2不给分
【解析】
根据浓盐酸具有挥发性分析;
[实验验证]
(1)根据氢氧化钙遇二氧化碳变浑浊,遇无色酚酞变红色分析;
(2)①根据稀盐酸和氢氧化钙反应生成氯化钙和水分析;
②根据氯化氢气体易溶于水,酸与紫色石蕊变红色分析;
(3)根据A点的pH大于10,二氧化碳和氢氧化钙反应生成碳酸钙和水分析;
(1)浓盐酸具有挥发性,使得制取的二氧化碳中含有氯化氢气体,导致石灰水不变浑浊。
(2)石灰水没有变质,说明溶液中含有氢氧化钙,可以用导管向澄清石灰水中吹气进行验证,也可以向石灰水中滴加无色酚酞溶液,因为有氢氧化钙,所以溶液会变红色的;
(3)①澄清石灰水未变浑浊的原因是二氧化碳中含有氯化氢气体,氯化氢气体溶于水形成盐酸,盐酸和氢氧化钙反应生成氯化钙和水,方程式是2HCl+Ca(OH)2=CaCl2+2H2O;
②氯化氢易溶于水,因此装置B的作用是吸收氯化氢气体,形成稀盐酸,因此溶液是酸性的,滴加紫色石蕊溶液后,溶液会变红色,B是氯化氢的水溶液,形成溶质是氯化氢;
(4)A点的pH 大于10,根据A点距10的距离,因此A的点的pH可以是12或14;AB段pH下降较快的原因是二氧化碳和氢氧化钙发生了反应,反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;已知BC段反应生成的是可溶于水的碳酸氢钙的过程。D点的溶液呈酸性因此,溶质是Ca(HCO3)2、H2CO3;
故答案为:猜想③:可能是二氧化碳中的氯化氢气体导致石灰水不浑浊。(1)用导管向澄清石灰水中吹气(或滴加酚酞溶液变红等合理答案也可);(2)①2HCl+Ca(OH)2=CaCl2+2H2O;②吸收氯化氢气体; 紫色石蕊溶液变红;HCl(填HCl、H2CO3或HCl、H2CO3、CO2,也给分,但是没有HCl不给分)。(3)①填12或14; CO2+Ca(OH)2=CaCO3↓+H2O;②Ca(HCO3)2、H2CO3;或填H2CO3给分,但是只填Ca(HCO3) 2不给分;


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:初中化学 来源: 题型:
【题目】单质及化合物是中学化学学习和研究的重要内容。
(1)如图为钠的原子结构示意图。下列说法不正确的是_________。

A X=1 B 钠原子的中子数为11
C 钠离子的符号为Na D 钠元素位于元素周期表中第三周期
(2)如图所示,用“W”型玻璃管进行微型实验。

①b处发生的现象是_____________;②写出a处发生反应的化学方程式___________;③写出为a处发生反应提供热量的化学反应方程式________
(3)浓硫酸和浓盐酸敞口放置均会变稀的原因________?
(4)已知:2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2↑。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象________?如何检验验证该水溶液中含有的两种溶质________。(简要写出实验步骤及现象)
(5)某同学为了测定氢氧化钠变质情况,取该样品固体20g,向其中加入足量的水,充分溶解;再加入足量的氯化钡溶液,充分反应后,过滤、洗涤、烘干,称得沉淀的质量为19.7g。计算该样品中氢氧化钠的质量分数________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验:
(1)甲同学实验操作如下:
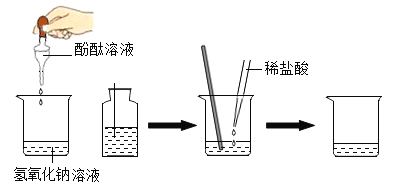
在烧杯中加入约5 mL氢氧化钠溶液、滴入几滴无色酚酞溶液,此时溶液呈________色。接着用滴管滴入一定量的稀盐酸,再用玻璃棒____________,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为________________________。
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究。
(实验探究)反应后溶液中的溶质是什么?
猜想一:只有NaCl
猜想二:NaCl和HCl
猜想三:NaCl和NaOH
以上猜想中,你觉得不合理的是________________。
为了验证另外两种猜想,乙同学设计如下实验方案。
实验操作 | 实验现象 | 实验结论 |
取少量反应后的溶液于试管中滴入Na2CO3溶液 | ________ | 猜想二成立 |
(反思交流)实验结束后,废液处理方法正确的是______(填序号)。
A 倒入下水道 B 倒入废液缸 C 带出实验室
(拓展延伸)乙同学再设计一个验证猜想二的实验:取少量反应后的溶液于试管中加入少量氧化铜粉末,若________________________,猜想二成立。
(3)用溶质质量分数为5%的NaOH溶液完全中和73 g10%的稀盐酸,需NaOH溶液多少克________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质甲、乙、丙的溶解度曲线如图所示。下列说法错误的是
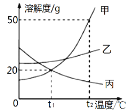
A. t1℃时,甲、丙饱和溶液的溶质质量分数都是16.7%
B. 使甲从溶液中结晶,只能用冷却热饱和溶液的方法
C. t2℃时150 g甲的饱和溶液降温到t1℃,能析出30g晶体
D. 将t2℃的三种物质饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系是乙>甲>丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小红利用氧气、二氧化碳传感器在装有两支燃着的高低蜡烛的密闭容器内顶部测容器内两支蜡烛从点燃到全部熄灭后,氧气(上)和二氧化碳(下)的浓度变化,如图所示。最终剩余氧气浓度15.65%,CO2浓度1.89%.则下列说法不正确的是( )

A. 支持蜡烛燃烧的氧气浓度须达到21%
B. 点B时两支蜡烛全部熄灭
C. 曲线BC段因为蜡烛熄灭,温度下降,二氧化碳密度大下沉,氧气上浮
D. 容器内高的蜡烛先熄灭矮的蜡烛后熄灭
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水在生活、生产和科学实验中非常重要,请回答下列问题。
(1)下列有关水的说法正确的是____。
A.活性炭可以吸附水中的异味 B.生活中常用煮沸的方法软化硬水
C.生活污水可以任意排放 D.经处理后的工业用水可以循环使用
(2)用如图所示装置进行可燃物燃烧条件的探究实验,已知白磷的着火点为40℃,红磷的着火点为240℃(白磷、红磷均不超过绿豆大小,锥形瓶中的白磷A与红磷被铜条隔开)。
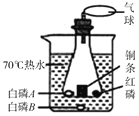
①写出锥形瓶中发生反应的化学方程式____。
②能得到“可燃物燃烧需要氧气”这一结论的现象为____。
③该实验中热水的作用____。
(3)根据铜锈蚀生成铜绿[Cu2(OH)2CO3],某同学猜想:铜锈蚀时要有氧气、水和二氧化碳共同参与。为证明铜生锈“必须有水参与”,需要进行下图所示实验中的________。
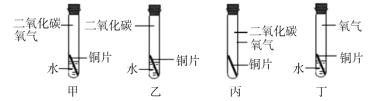
(4)不同温度下,二氧化碳在水中的溶解度随压强的变化如右图所示。图中t1对应的温度为20℃,则t2对应的温度____(填字母)。
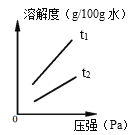
A.大于20℃ B.小于20℃ C.无法确定
(5)按如图所示装置,将液体x注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是____。
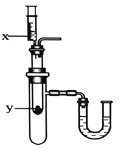
选项 | x | y |
A | 稀盐酸 | 镁 |
B | 水 | 氧化钙 |
C | 水 | 硝酸铵 |
D | 水 | 氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明同学对家中久置的袋装固体食品防腐剂的成分产生了兴趣(品名和成分如图所示),于是和同学一起,设计实验进行探究:

[提出问题]久置固体食品防腐剂的成分是什么?
[查阅资料]铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
[作出猜想]久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 。
[实验探究]甲同学的探究方案如下表:
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有_______和氢氧化钙。此过程的化学方程式_______。 |
(2)另取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有Fe ,一定不含 Fe2O3 |
(3)将步骤(2)中产生的气体通入到澄清的石灰水中 | ________ | 固体中一定含有CaCO3 |
[交流与反思]
(1)“504双吸剂”中的铁粉可以吸收空气中的_______、______。
(2)实验操作(2)的实验现象里“有大量无色气体产生”, 根据甲同学的整体探究方案推测,无色气体的成分是一定含有______,可能含有________。
(3)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是______。
(4)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校的学习小组根据下面给出实验装置(另有托盘天平可用),粗略测定铜锌合金(黄铜)中锌的质量分数(黄铜已加工成粉末)。
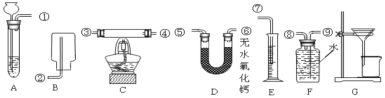
(分析思考)
同学们通过充分“交流-分析-讨论”后一致认为,设计以下三种实验方案均可测出黄铜中锌的质量分数。同学们用过量稀硫酸与称取的 a克黄铜粉样品进行充分反应后,实验中测定了以下数据:
①测定生成H2的体积b升(已知氢气的密度为ρ)。
②过滤、洗涤、烘干后,测定漏斗中剩余固体的纯净质量为c克。
③充分反应后,测定 A 装置中仪器和药品总质量减少了d克。
(方案一)小悦仅选用一个实验装置 A 进行实验,并用测定的数据,通过计算,求出黄铜中锌的质量分数为____。
(方案二)小华选用两个装置__(填装置编号)进行实验,并用数据__(填数据编号),通过计算也求出了黄铜中锌的质量分数。
(方案三)小琳选用三个实验装置进行实验,装置连接的顺序是(用装置接口处的编号表示)__,并用测定的数据,通过计算也求出了黄铜中锌的质量分数。
(反思评价)小组对上述三种实验方案进行了综合评价,认为方案___最简单易行。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,在小烧杯乙和丙中分别放入不同的物质后,立即用大烧杯甲罩住小烧杯乙和丙。下列有关说法错误的是
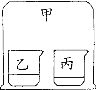
A.乙和丙中分别放入浓盐酸和浓氨水后,大烧杯甲中会有白烟产生
B.乙和丙中分别放入浓氨水和酚酞试液后,丙中酚酞试液会变红
C.乙和丙中分别放入浓盐酸和硝酸银溶液后,乙中产生白色沉淀
D.乙和丙中分别放入水和浓硫酸后,丙中溶质的质量分数会减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com