
分析 ①根据自来水生产过程中能凝聚水中悬浮物的是明矾解答;
②根据活性炭具有吸附性解答;
③根据常作气体燃料的一种有机物是甲烷解答;
④根据氧化钙具有吸水性解答;
⑤根据氧气能够支持燃烧解答;
解答 解:
①明矾可以吸附较大可以,加速沉降,故自来水生产过程中能凝聚水中悬浮物的是明矾;
②用活性炭去除冰箱中的异味是利用了活性炭具有吸附性;
③常作气体燃料的一种有机物是甲烷;
④氧化钙具有吸水性,可以做食品干燥剂;
⑤氧气能够支持燃烧,能使带火星的木条复燃;该气体在空气中的体积分数约为$\frac{1}{5}$.
答案:
①明矾;
②吸附;
③CH4;
④CaO;
⑤氧气(或O2); $\frac{1}{5}$;
点评 本题难度不大,熟练掌握常见物质的性质、用途是正确解答此类题的关键所在.


科目:初中化学 来源: 题型:选择题
| A. | 实验中取用的剩余药品应放回原瓶 | |
| B. | 加热后的试管可以放在桌面上自然冷却 | |
| C. | 进行过滤操作时,玻璃棒只可接触三层滤纸一侧 | |
| D. | 使用滴瓶滴加试剂后,立即用蒸馏水洗净滴管并放回原瓶 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石墨作铅笔芯 | B. | 生石灰作干燥剂 | C. | N2作保护气 | D. | CO2作灭火剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 组成:都是由碳和氧两种元素组成,但二氧化碳比一氧化碳多一个氧元素 | |
| B. | 性质:都能溶于水,但是CO能燃烧而CO2不能 | |
| C. | 用途:CO2可用于光合作用、灭火等;CO可作气体燃料,冶炼金属等 | |
| D. | 危害:都有毒性,CO2 还会造成温室效应 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 石墨能导电,可作电极 | B. | 干冰气化吸热,可用于保藏食品 | ||
| C. | 氧气有助燃性,可用于炼钢和气焊 | D. | 稀有气体性质稳定,可制成霓虹灯 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
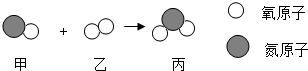
| A. | 消耗的甲和乙的分子个数比为2:1 | B. | 甲中元素存在形态为游离态 | ||
| C. | 该反应涉及三种氧化物 | D. | 反应前后分子总数不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |

| 装置B | 装置C | 装置D | |
| 实验前物质的质量/g | 180.0 | 200.0 | 122.2 |
| 实验后物质的质量/g | 176.9 | 201.5 | 124.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com