
下列叙述、对应的化学方程式和所属反应类型正确的是
A. 拉瓦锡研究空气成分 2HgO =2Hg+O2↑ 分解反应
B. 探究一氧化碳的还原性 CO+CuO Cu+CO2 置换反应
Cu+CO2 置换反应
C. 用二氧化碳制作碳酸饮料 CO2↑ + H2O ═ H2CO3 化合反应
D. 用含小苏打的药物治疗胃酸过多 NaHCO3+HCl═NaCl+H2O+ CO2↑ 复分解反应
D 【解析】书写化学方程式的步骤一般有四步:1.根据实验事实,在式子的左、右两边分别写出反应物和生成物的化学式,并在式子的左、右两边之间画一条短线;当反应物或生成物有多种时,中间用加号(即“+”)连接起来。2.配平化学方程式,并检查后,将刚才画的短线改写成等号(表示式子左、右两边每一种元素原子的总数相等)。3.标明化学反应发生的条件(因为化学反应只有在一定的条件下才能发生);如点燃、加热(常... 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:重庆市江津区2018届九年级下学期六校联考化学试卷 题型:填空题
甲、乙、丙三种物质的溶解度曲线如下图所示,根据图中信息回答下列问题:
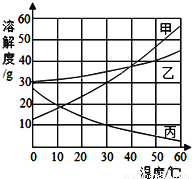
(1)50℃时,乙物质的溶解度是_________g。
(2)50℃时,将40g乙物质放入100g水中充分溶解后,所得溶液的溶质质量分数为______(精确到0.1%)。
(3)要使50℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是______。
(4)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液的溶质质量分数由大到小的顺序为______________。
40; 28.6%; 加入甲(或恒温蒸发水); 乙>甲>丙 【解析】(1)在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。50℃时,乙物质的溶解度是40g。(2)溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。50℃时,乙的溶解度为40g,将40g乙物质放入100g水中充分溶解后,所得溶液的溶质质量分数为40g÷(100g+40g)×100%≈28.6%;(3)由图可知,甲...查看答案和解析>>
科目:初中化学 来源:广州市白云区2018届九年级中考一模化学试卷 题型:单选题
硒Se,可以用作光敏材料、电解锰行业催化剂、动物体必需的营养元素和植物有益的营养元素等。其在周期表中的信息及原子结构示意图如图所示。下列对于硒的说法的错误是
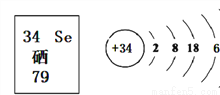
A. 硒离子符号是Se2-
B. 硒的相对原子质量是79
C. 硒在反应中易失电子
D. 硒的化学性质与硫相似
C 【解析】A. 硒原子最外层有6个电子,易得到2个电子,带2个单位的负电荷,所以离子符号是Se2-,正确;B. 硒的相对原子质量是79,正确;C. 硒在反应中易得到2个电子,达到最外层是8个电子的稳定结构,错误;D. 硒、硫两种原子的最外层电子个数相同,因此它们的化学性质相似,正确。故选C。查看答案和解析>>
科目:初中化学 来源:福建省厦门市2017届九年级全市中考模拟化学试卷 题型:单选题
在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。下列关于此反应的认识正确的是
物 质 | X | Y | Z | W |
反应前的质量/g | 20 | m | 16 | 14 |
反应后的质量/g | 4 | 6 | 60 | 50 |
A. 参加反应的X与Y的质量比为1︰4
B. 若W为水,则X或Y必定为酸或碱
C. m的数值为64
D. 若X为化合物,Y为单质,则该反应一定为置换反应
A 【解析】由表中数据分析可知,反应前后X的质量减少了20g-4g=16g,故X是反应物,参加反应的X的质量为16g;同理可以确定Z是生成物,生成的Z的质量为60g-16g=44g;W是生成物,生成的W的质量为50g-14g=36g;A、参加反应的X与Y的质量比为16g:64g=1:4,故选项说法正确;B、该反应的反应物为X和Y,生成物是W和Z,若W为水,由于无法确定X、Y的元素组成,X或Y...查看答案和解析>>
科目:初中化学 来源:四川省绵阳市游仙区2018届九年级下学期二诊化学试卷 题型:综合题
(1)某兴趣小组准备通过锌与稀硫酸反应产生的氢气来测定稀硫酸中溶质的质量分数,装置如下:

①小明同学用如图1所示装置进行实验,你认为他应该选择的最简易的装置及其连接顺序是:A→______→ D。
②小明若用图2装置收集氢气,应选择集气装置____(填“A”或“B”),为保证测量结果的准确性,收集气体的时机是_________。
a.导管口还没有气泡产生时
b.导管口连续均匀冒出气泡时
c.导管口冒出气泡很多时
③小张同学用如图3所示装置进行了实验:
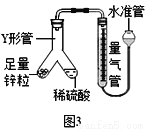
Ⅰ.下列能说明装置气密性良好的是_________。
A.连接仪器后,向水准管中注水,直至左右两边管内形成稳定高度差。
B.向水准管内注水,连接好左侧装置,抬高水准管,左右两边液面始终相平。
Ⅱ.反应完毕后,每间隔1分钟读取气体体积、气体体积逐渐减小,直至体积不变。气体体积逐渐减小的原因是_________________(排除仪器和实验操作的影响因素)。
Ⅲ.若实验中测得稀硫酸的溶质质量分数偏大,下列可能的原因是____________。
a.装置漏气 b.读取数据时水准管的水面高于量气管的水面
c.未待冷却就读取量气管读数
(2)在金属活动性顺序表中,排在前面的金属能把位于后面的金属从它的盐溶液中置换出来,但小明在做金属钠与硫酸铜溶液反应的实验时,却出现了异常现象。
【进行实验】取一块绿豆大小的金属钠,放入盛有20毫升硫酸铜溶液的小烧杯中,发现金属钠浮在液面上不停打转,产生大量气体,烧杯发烫,溶液中出现了蓝色絮状沉淀,一会儿部分沉淀渐渐变黑,将反应后烧杯中的混合物进行过滤,得滤渣和无色滤液。
【提出问题】①生成的气体是什么?
②滤渣的成分是什么?
③无色滤液中的溶质是什么?
【查阅资料】①钠能与水反应生成一种碱,同时放出气体。
②氢氧化铜受热至60~80℃变暗,温度再高分解为相应的金属氧化物(化合价不变)和水。
【实验探究一】 探究生成的气体是什么?
小明将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,把气体通入肥皂水中,将燃着的木条靠近飘起的肥皂泡,有爆鸣声。说明生成的气体是___________。
【实验探究二】 探究滤渣的成分是什么?
【猜想假设】滤渣中含有Cu(OH)2和_____________,还可能含有Cu。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量滤渣,向其中加入足量的稀硫酸 | ____________________ | 滤渣中没有Cu |
【实验结论】通过实验,小明同学得出结论:钠加入到硫酸铜溶液中会先与水反应,生成物再与硫酸铜反应生成氢氧化铜。请写出上述发生的两个反应的化学方程式______________ ,________________。
【实验探究三】探究无色滤液的溶质是什么?
【猜想假设】猜想① Na2SO4 , 猜想②________________。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量无色滤液,向其中加入__________ | 无明显变化 | 猜想①成立 |
【反思交流】钠加入硫酸铜溶液中出现黑色物质的可能原因是(用化学方程式表示)_________。
C B a A 反应放热、气体在冷却过程中体积逐渐减小 c H2 CuO 固体全部溶解、溶液变成蓝色 2Na + 2H2O = 2NaOH + H2↑ CuSO4+2NaOH = Cu(OH)2↓+Na2SO4 Na2SO4和NaOH 无色酚酞试液 Cu(OH)2CuO + H2O 【解析】①最简易的装置及其连接顺序是:A→C→ D。用C收集氢气,同时通过读取压入D中水的体积,测定收集到氢气...查看答案和解析>>
科目:初中化学 来源:四川省绵阳市游仙区2018届九年级下学期二诊化学试卷 题型:单选题
下列有关实验的叙述中,正确的是( )
A. 验证氧气的性质时,把红热的木炭插入盛有氧气的集气瓶,要由瓶口向下快速插入
B. 把1~2小粒碘分别投入5mL水、5mL汽油中,振荡,观察到碘几乎不溶于汽油
C. 把等量的肥皂水分别滴加到等量的软水、硬水中,振荡,观察到软水中产生较多泡沫
D. 把乒乓球碎片和滤纸碎片分开放在一块薄铜片的两侧,加热铜片的中部,滤纸先燃烧
C 【解析】A.根据木炭在氧气中燃烧的实验操作判断; B. 根据碘几乎不溶于水,却可以溶解在汽油中,进行分析判断; C. 根据硬水与软水的检验方法进行分析解答即可; D.根据物质燃烧时着火点分析; 【解析】 A.把红热的木炭插入盛有氧气的集气瓶时,应由瓶口向下慢慢插入,现象明显,该选项不正确; B. 把1~2小粒碘分别投入5mL水、5mL汽油中,振荡,观察到碘...查看答案和解析>>
科目:初中化学 来源:安徽省皖北十校2018届九年级下学期联考化学试卷 题型:单选题
下图是物质A、B的溶解度曲线,下列说法正确的是
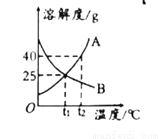
A. 两种物质的溶解度都随温度的升高而增大
B. t2℃时,将溶液A、B降温至t1℃都有晶体析出
C. t1℃时,溶液A、B的溶质质量分数一定相等
D. t2℃时,所配溶液A的溶质质量分数不超过28.6%
D 【解析】A、由图可知,B物质的溶解度随温度的升高而降低,错误;B、A物质的溶解度随温度的升高而增大,t2℃时,溶液A是否饱和不确定,故t2℃时,将溶液A降温至t1℃时,无法判断是否有晶体析出。B物质的溶解度随温度的升高而降低,故t2℃时,将溶液B降温至t1℃时,无晶体析出,错误;C、由图可知,t1℃时A、B的溶解度相等。t1℃时,溶液A、B是否饱和无法确定。故t1℃时,溶液A、B的溶质质...查看答案和解析>>
科目:初中化学 来源:山东省泰安市岱岳区2017-2018学年八年级下学期期中考试化学试卷 题型:单选题
氢氟酸(HF)对玻璃有腐蚀作用,可用在玻璃上雕刻各种精美图案,也可用在玻璃仪器上标注刻度及文字。氢氟酸与玻璃发生的反应可以表示为:SiO2+4HF=X↑+2H2O,关于物质X的组成,下列说法正确的是
A. 可能含有氢元素 B. 可能含有氧元素
C. 一定含有硅元素、氟元素 D. X是一种氧化物
C 【解析】试题分析:根据化学变化前后原子的种类、数目不变,可判断物质X的分子由1个Si原子和4个F原子构成,则物质X的化学式可表示为SiF4;物质X由硅、氟两种元素组成,故C正确;物质X中不含H、O元素,不属于氧化物,故A、B、D不正确;故选C.查看答案和解析>>
科目:初中化学 来源:四川省成都市成华区2018届九年级二诊考试化学试卷 题型:科学探究题
某校化学活动小组用镁和铁探究金属的反应规律。
【查阅资料】
①镁,铁的活动性均在 H 之前并且镁比铁活泼。
②相同条件下,相同时间内金属的活动性越强,与酸反应越剧烈,产生的氢气越多。
【探究一】在室温条件下进行如图所示实验。试管内的镁带和铁片表面均被打磨洁净,且形 状、大小相同;同时加入等质量和等浓度的稀盐酸。
(1)该兴趣小组的同学认为该方案中长颈漏斗起非常重要的作用。
①通过相同条件下,相同时间内长颈漏斗中 __________
②长颈漏斗在实验中还可以起_________________ 作用。
(2)在甲、乙装置的水中滴入 2~3 滴红墨水的目的_______________。
(3)乙装置中反应方程式为______________,该反应属于基本反应类型中的_______反应。
(4)观察到甲装置中产生气泡速率比乙装置快或 __________现象时,都可以证明镁的金属活动性比铁的强。
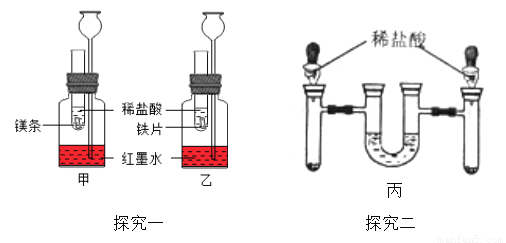
【探究二】方案二:如图丙,将等质量光亮洁净,形状厚薄相同的镁条和铁片分别放入左、 右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U 型管内为水,初始液面相平,反应过程中装置气密性良好)。
(5)实验过程中 U 型管中液面 _______(填“左高右低”,“左低右高”,“相平”); 充分反应后,冷却到室温 U 型管中液面 ___________填“左高右低”,“左低右高”,“相平”),原因是_____。
【探究三】在硫酸铜和硫酸亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出 的固体中滴加稀硫酸,没有气泡产生。下列判断正确的是 ________。写成发生反应的化学方程式 ________ 。
A.滤出的固体中一定含有铜 B.滤出的固体可能含有铁和镁
C.滤液中可能含有硫酸铜 D.滤液中一定含有硫酸镁和硫酸亚铁
液面的高低 平衡内外压强 便于观察实验现象 Fe + 2HCl = H2↑ + FeCl2; 置换 甲中长颈漏斗的液面比乙中高 左低右高 ; 相平; 金属均有剩余,充分反应后生成的 H2 质量相等 A,B ; Mg + CuSO4 = Cu + MgSO4 【解析】镁和铁探究金属的反应规律。镁,铁的活动性均在 H 之前并且镁比铁活泼,镁和铁均可与盐酸或硫酸反应。相同条件下,相同时间内金属的活...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com