
����Ŀ�������г������ʵ����ʡ��Ʒ����ǻ�ѧ�о�����Ҫ���ݣ�
��1�����Ϸ�Ӧ������������϶�������_____����������������������������
��2������ˮ��Ӧ�����������ƺ���������ѧ����ʽΪ_____��
����ʵ�������в������ڼ��ȵ���_____������ĸ���ţ���
a �ձ� b ��Ͳ c �Թ� d ������
��3��ij��ѧС��ѡ������װ�ú�ҩƷ����̽��ʵ�飮
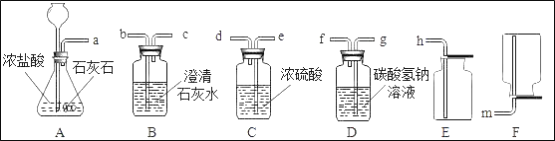
��A�з�Ӧ�Ļ�ѧ����ʽΪ_____��
������A��B���ӣ�A�в��������岢����ʹB�е���Һ����ǣ�����Ϊʲô_____��
��4����ͼװ�ÿ���һ����̼��ԭ��������ʵ�飬���������ɵ�������
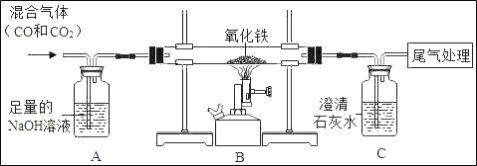
��Bװ�ò�������ɹ۲쵽��������_____��
��Cװ���з�Ӧ�Ļ�ѧ����ʽΪ_____��
��5����ҵ�Ͽ����������ȷ�Ӧ�����Ӹֹ졢ұ�����۽����ȣ���ԭ�����ڸ�����������ijЩ�����������������û���������������������������Ӧ����ȡ25.2kg������������Ҫ�������������Ƕ���_____��
���𰸡����� 2Na+2H2O��2NaOH+H2�� b CaCO3+2HCl�TCaCl2+H2O+CO2�� ����A��ʹ�õ���Ũ���ᣬ���Ե������ɵĶ�����̼�к��д�����HCl���� ��ɫ��ĩ��ɺ�ɫ CO2+Ca��OH��2��CaCO3��+H2O 10.8kg
��������
��1�����ݻ��Ϸ�Ӧ�����ֻ����������ϵ���������һ�����ʣ�����������һ���ǻ����
��2�����ݸ����ķ�Ӧ�����������д��Ӧ�Ļ�ѧʽ��ע��Ҫ��ƽ����Ϥ�����Ŀ��Ա����ȵ�������ֱ�ӱ����ȵ�������
��3����Ϥ��ס������̼������Ʊ��ͼ����Լ����е����ʣ�
��4����Ϥһ����̼��ԭ��������ʵ���Լ���Ӧ����������ļ��飻
��5�����ݶ�Ӧ�Ļ�ѧ����ʽ�������������������ĵ���������������Ĺؼ��Ǹ�����Ϣ��д��Ӧ�Ļ�ѧ����ʽ��
��1�����Ϸ�Ӧ�����ֻ�������������������һ�����ʵģ����Զ�Ӧ��������ֻ���ǻ�����������ǵ��ʣ�
��2������ˮ��Ӧ�����������ƺ���������Ӧ��Ϊ�ƺ�ˮ��������ʱ�������ƺ���������Ӧ�Ļ�ѧ����ʽΪ 2Na+2H2O��2NaOH+H2����
a���ձ����Լ��ȣ�������Ҫ��ʯ�������ϣ�
b����Ͳ�����Ա����ȣ�Ҳ����ʢ���ȵ�Һ�壻
c���Թܣ����Ա�ֱ�Ӽ��ȣ�
d���������Ա�ֱ�Ӽ��ȣ�
��3��
��A����ʯ��ʯ����Ҫ�ɷ�̼��ƺ����ᷴӦ�������Ȼ��ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ CaCO3+2HCl�TCaCl2+H2O+CO2����
������A��B���ӣ�����A��ʹ�õ���Ũ���ᣬ���Ե������ɵĶ�����̼�к��д�����HCl���ʣ��������岢����ʹB�е���Һ����ǣ�
��4��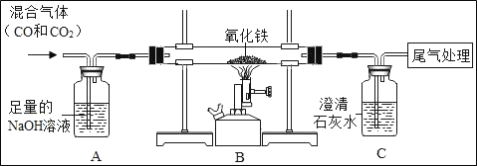
��Bװ�ò�������ɹ۲쵽�������� ��ɫ��ĩ��ɺ�ɫ��
��Cװ�ü������������ж�����̼�ģ����Զ�Ӧ�Ļ�ѧ����ʽΪ CO2+Ca��OH��2��CaCO3��+H2O��
��5��������������ijЩ�����������������û���������������������������Ӧ����ȡ25.2kg�������Զ�Ӧ�Ļ�ѧԭ�������ڸ��µ�������������������Ӧ������������������Ӧ�Ļ�ѧ����ʽΪ��8Al+3Fe3O4![]() 4Al2O3+9Fe����ƽʱ����С��������������Ԫ�����֣���
4Al2O3+9Fe����ƽʱ����С��������������Ԫ�����֣���
����������Ҫ��������������x

![]() x��10.8kg
x��10.8kg


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ���һ����Ҫ�Ļ���ԭ�ϡ�����ͨ�����ַ�����ȡ�Ҵ���
�������ͷ��������۵�ũ��Ʒ������ࡢ�����Ұ��ֲ���ʵ�ȣ������ú���ά�ص�ľм��ֲ�ᆬ�ѵȡ���Щ���ʾ�һ����Ԥ������ˮ�⡢���ͣ������Ƶ��Ҵ�����һ��������______�仯������������������ѧ������
������ϩˮ�������÷�Ӧ����ʾ��ͼ���£�
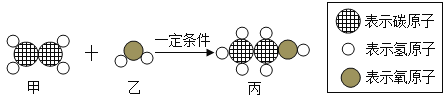
��д����Ӧ�Ļ�ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ճ������ũҵ�����벻��ˮ����ش�
��1��ˮ_____������ڡ������ڡ�������������������Ӫ����֮һ��
��2�����н϶�����Ըơ�þ�������ˮ����_____�����ˮ����Ӳˮ������
��3�����о���ˮ�ĵ�һ�����У���Ծ����̶Ƚϸߵ���_____������ĸ����
A ���� B �������� C ����
��4��ˮ��ͨ��������¿��Էֽ⣬д���÷�Ӧ�Ļ�ѧ����ʽ_____��
��5���ס��ҡ������ֹ������ʵ��ܽ��������ͼ��ʾ���ش��������⣺
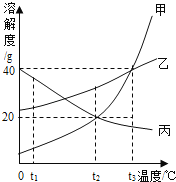
��t1��ʱ�����ܽ��_____�����ܽ�ȣ����������������������
��t2��ʱ����15g�����ʼ��뵽ʢ��l00gˮ���ձ��У�����ܽ��������Һ�Ǽ����ʵ�_____��Һ������͡������͡�����
��t3��ʱ�����ס��ҡ����������ʵı�����Һͬʱ���µ�t1�棬������Һ�����ʵ����������ɴ�С��˳����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���������ϡ�����ȡij����������ͭп����Ҫ�ɷ�ΪCuO��ZnO������ɷּȲ����ᷴӦ��Ҳ���ܽ���ˮ���ķ�����ʵ�ַ����ۺ����á�����ʵ���������£�
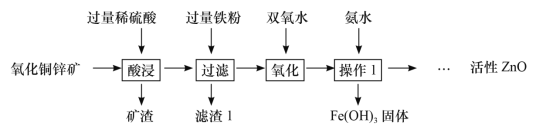
���������ʵ�����̻ش��������⣺
��1������1��������_____��
��2��������ͭп���м������ϡ���ᣬ��ַ�Ӧ����Һ�е�����Ϊ_____��
��3���ӹ������ۣ�������Ӧ�Ļ�ѧ����ʽΪ_____��
��4����ʵ������У�˫��ˮ����![]() ��Ӧ����
��Ӧ����![]() ��ˮ���Ա��ں����IJ����н���Һ����Ԫ�س�ȥ�����������ҺҲ�ܽ�
��ˮ���Ա��ں����IJ����н���Һ����Ԫ�س�ȥ�����������ҺҲ�ܽ�![]() ������
������![]() �������ɿ����Ե����Σ�ѡ��˫��ˮ���ŵ���_____��
�������ɿ����Ե����Σ�ѡ��˫��ˮ���ŵ���_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��FΪ���л�ѧ�������ʣ����Ƿֱ���H��C��O��Cl��Na��Ca�е�2��3��Ԫ����ɣ����������ƶϣ������������
��1��AΪ������������Ʊ��������������ļд����A�Ʊ���Ļ�ѧ����ʽ_____��
��2��B��C��ΪҺ�壬�����Ԫ����ͬ��C��һ�������¿�����B��B�Ļ�ѧʽΪ_____��
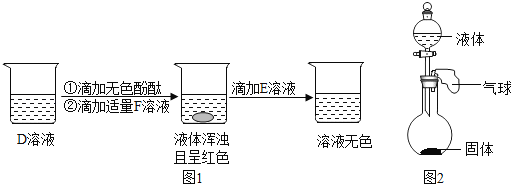
��3��D��һ�ֳ����Σ������ڲ�������ֽ����֯��ϴ�Ӽ���������ȡD��Һ����ʵ�飬����������������ͼ1��ʾ��D��F��Ӧ�Ļ�ѧ����ʽΪ_____
��4�����������ƶϳ�����A��F����������ѡ2��Ϊһ�飬��ͼ2װ��ʵ�飬��������д������Ҫ������ʡ�
���� ���� | �����ģ�һ��ʱ���ָ�ԭ״ | �����ģ�һ��ʱ��ָ�ԭ״ |
Һ�� | ��_____ | ��_____ |
���� | ��_____ | ��_____ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵĺ�����ʡ��۹��ɣ���ṹ���ͱ�ʾ����֮�佨����ϵ���ǻ�ѧѧ�Ƶ��ص㡣����ͼʾ�ش��������⣺
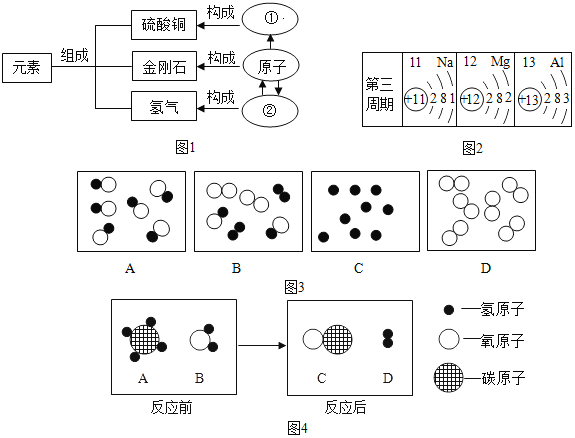
��1�����ʵ���ɼ����ɹ�ϵ��ͼ1��ʾ��ͼ������ʾ����_____������ʾ����_____��
��2��Ԫ�����ڱ���ѧϰ��ѧ����Ҫ���ߣ���ͼ2��Ԫ�����ڱ��е�������Ԫ��ԭ�ӽṹʾ��ͼ�����е�13��Ԫ������_____����������ǽ�������Ԫ�أ��ڻ�ѧ��Ӧ������_____���ʧȥ���õ��������ӣ��γ�_____�������ӷ��ţ���
��3����ͼ3�����и�ͼ�кͷֱ��ʾ���ֲ�ͬԪ�ص�ԭ�ӣ������б�ʾ��������_____��ʾ���ʵ���_____����ʾ���������_____��
��4��A��B��C��D��ʾ���������У��ڸ��������£�A��B��Ӧ����C��D����ʾ��ͼ�磬4��ʾ����Ӧ������C��D�������ʵ�������Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��̽��ϡ���������������Һ�ķ�Ӧ���̡�����ձ�����Һ��pH��μ�Һ������仯��������ͼ��ʾ������˵������ȷ���ǣ�������
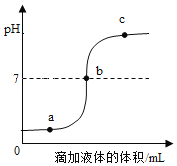
A.��pH�仯���̿���֤����ͼ���˻�ѧ��Ӧ
B.ͼ��a����ʾ��Һ�У����е��������Ȼ��ƺ��Ȼ���
C.��ͼ��c����ʾ��Һ�еμ���ɫʯ���Һ��Ϊ��ɫ
D.��ʵ���ǽ�����������ε��뵽ʢ��������Һ���ձ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������һƿ��ǩ��ȱ����ƿ��û����ȫ�ܷ����ɫ��Һ������ͼ����Ϊȷ�����е����ʣ�ͬѧ�ǽ��������µ�̽�����������뵽����ȥ���ش��й����⡣
�����в��롿�������Һ��������NaCl��
�������Һ��������NaOH��
�������Һ��������Na2CO3��
����IV������Һ��������NaHCO3.
���������ϡ����������ʵ������Ϣ���±���
���� | NaCl | NaOH | Na2CO3 | NaHCO3 |
�����µ��ܽ��/g | 36 | 109 | 21.5 | 9.6 |
������ϡ��Һ��pH | 7 | 13 | 11 | 9 |
�����ʵ������Ϣ��֪������Һ�����ʲ���NaHCO3����Ϊ������NaHCO3��Һ���ʵ��������������
����ȷ��01.%����
������ʵ�顿
��1���ⶨ��Һ��pH����7������Һ�����ʲ��� ���ѧʽ����
��2��ͬѧ���ֽ���������ʵ�飬ʵ��������£�
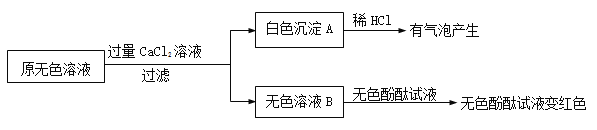
��������ɫ�����Ļ�ѧ����ʽ�� ��
��ʵ������ж�ԭ��ɫ��Һ�к��е������� ��
����ý��ۡ�
��ƿԭ��װ����ɫ��Һ��������NaOH������ ���û�С��������֡���ȫ���������ʡ�
����չ��
�ᴿ����ɫ��Һ�IJ����ǣ�������ɫ��Һ�м��������� ��Ȼ����ˡ���Ӧ��ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɽ��ˮ�к��д�����H2SO4��CuSO4��ֱ���ŷŻ�Ӱ��ˮ������ԣ�������ؽ�����Ⱦ��ͨ���������Ի��ս���ͭ����ʹ��ˮpH���ؽ��������ﵽ�ŷű���

��֪�����������ɫ�������ɡ�
��1�������Ͳ��������еIJ�����_____��
��2�������õ�����ͭ�ķ�Ӧ�Ļ�ѧ����ʽΪ_____���÷�Ӧ�ܷ�����ԭ����_____��
��3������Ca��OH��2���Խ�����м����������ԭ����_____�����������ֽ��ͣ�
��4������������Na2S���ɴ��Ʋ��ˮ�۲�������Ҫԭ�������к���_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com