
分析 根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析.
解答 解:镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为:加过量的BaCl2溶液,加过量的Na2CO3溶液,加过量的NaOH溶液,过滤,加适量的盐酸;或者,加过量的NaOH溶液,加过量的BaCl2溶液,加过量的Na2CO3溶液,过滤,加适量的盐酸或加过量的BaCl2溶液,加过量的NaOH溶液,加过量的Na2CO3溶液,过滤,加适量的盐酸;故操作顺序为:②④⑤①③或⑤②④①③或②⑤④①③;
(3)由于在上述操作中通过过滤得到的滤液中含有氢氧化钠和碳酸钠,加入适量盐酸将滤液中的氢氧化钠和碳酸钠转化为氯化钠,得到纯净的氯化钠溶液,反应的方程式分别为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;NaOH+HCl═NaCl+H2O;
故答案为:除去过量的碳酸钠和氢氧化钠;Na2CO3+2HCl═2NaCl+H2O+CO2↑;NaOH+HCl═NaCl+H2O.
点评 本题主要考查了在粗盐提纯中的物质的除杂或净化操作,在解此类题时,首先要了解需要除去的是哪些离子,然后选择适当的试剂进行除杂,在除杂质时,杂质和所加的试剂的状态一样,就要注意,加入的量的控制.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
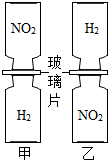 把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )| A. | 分子总是不断运动的 | |
| B. | 甲乙现象的差异与气体的密度有关 | |
| C. | 常温常压下,NO2的密度大于H2的密度 | |
| D. | 分子本身都是有大小的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:
如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
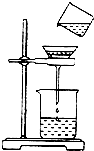 如图是明明同学将浑浊的河水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,进行过滤的操作.
如图是明明同学将浑浊的河水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,进行过滤的操作.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | A | B | C | D |
| 肥皂水 | 食醋 | 牙膏 | 食盐水 | |
| pH | 10 | 3 | 9 | 7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
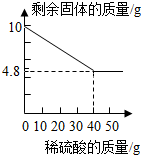 南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.
南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
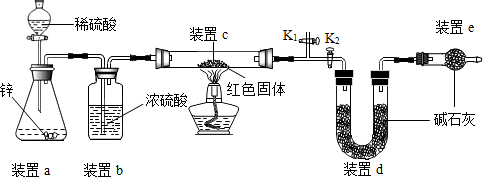
| 实验操作 | 实验现象 | 实验结论 |
| 取少量红色固体加入到足量稀硫酸溶液中 | 若无明显现象 | 假设1成立 |
| 若固体部分(选填“全部”或“部分”)溶解,溶液由无色变蓝色 | 假设2和假设3均成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaC1、K2SO4、Ba(No3)2在水中能大量共存 | |
| B. | 用水可以区分硝酸铵和氢氧化钠两种固体 | |
| C. | 除去稀HCl中少量的H2SO4,可以滴加适量的硝酸钡溶液,然后过滤 | |
| D. | 铜丝在空气中加热后质量会增加,该反应不遵守质量守恒定律 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com