
【题目】某化学兴趣小组为探究铁、铜、锌、银的金属活动性顺序。设计了如图所示的三个实验(其中金属均已打磨,且其形状、大小相同;所用盐酸的溶质质量分数、用量也相同)下列判断中,错误的是( )
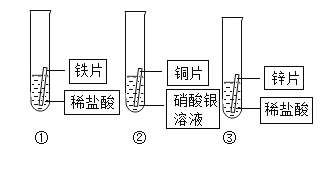
A.通过上述三个实验,不能判断出四种金属的活动性顺序
B.通过实验①和③的反应剧烈程度,可以判断出铁和锌的金属活动性强弱
C.若增加一个铜锌活动性比较的实验,则可判断出四种金属的活动性顺序
D.通过实验②的反应现象,可以判断出铜和银的金属活动性强弱
【答案】C
【解析】
A. 通过上述①和③两个实验,锌和铁与酸反应的剧烈程度可以比较锌铁的活动性强弱(锌>铁),通过②可以比较铜银的活动性强弱(铜>银),但是不能判断出铁和铜的活动性强弱,不能比较四种金属的活动性顺序。故A不符合题意;
B. 金属均已打磨,且其形状、大小相同;所用盐酸的溶质质量分数、用量也相同,通过实验①和③的反应剧烈程度,可以判断出铁和锌的金属活动性强弱。故B不符合题意;
C. 通过A的分析可知,若增加一个铜锌活动性比较的实验,只能比较锌铜的活动性,还是比较不出铁铜的活动性顺序,仍然不能判断出四种金属的活动性。故C符合题意;
D. 一种金属与另一种金属的盐溶液反应,如果能反应,金属单质的活动性比盐溶液中的金属活动性强,如果不反应,金属单质的活动性比盐溶液中的金属活动性弱,所以通过实验②的反应现象,可以判断出铜和银的金属活动性强弱。故D不符合题意。
故选C。


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:
【题目】小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂。于是,他对影响氯酸钾分解的因素及催化剂的催化效果产生了探究兴趣。
(提出问题)氧化铜是否比二氧化锰催化效果更好?影响氯酸钾分解速率的因素有哪些呢?
(设计实验)小雨以生成等体积的氧气为标准,设计了下列几组实验。
序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
① | 10.0g | 330℃ | 100mL | t1 | |
② | 10.0g | CuO1.5g | 330℃ | 100mL | t2 |
③ | 10.0g | MnO21.5g | 330℃ | 100mL | t3 |
④ | 10.0g | MnO2_____g | 380℃ | 100mL | t4 |
(1)若t1>t2,说明氧化铜能加快氯酸钾的分解速率。若要确定氧化铜是此反应的催化剂,还需探究反应前后,氧化铜的_____和_____不变。
(2)写出实验④所涉及的化学反应的文字表达式_____。
(3)实验④中MnO2的质量为_____g,若t3>t4,则化学反应快慢与温度的关系是_____。
(4)氯酸钾的分解速率可能还与_____因素有关,请设计实验证明_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是自来水厂净水过程示意图,回答下列问题:
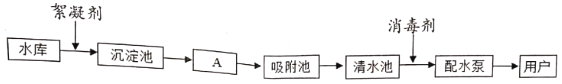
(1)除去水中有异味、有颜色的物质可加入________________。
(2)自来水厂常用二氧化氯作消毒剂,二氧化氯的化学式为_______________。
(3)通过上述流程所得到的自来水_________(填“一定”或“不一定”)是软水。实验室获得纯净水的方法常用_____________(填“煮沸”或“蒸馏”)方法。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3,其流程如下:

已知:(1)SiO2不溶于水也不溶于一般酸溶液。
(2)“还原”时,FeS2与H2SO4不反应,Fe2(SO4)3通过反应Ⅰ、Ⅱ被还原,反应Ⅰ:7Fe2(SO4)3+FeS2+8H2O=15FeSO4十8H2SO4,反应II:Fe2(SO4)3+FeS2=3FeSO4+2S↓。
回答下列问题:
(1)写出烧渣“酸溶”时发生反应的一个化学方程式________。
(2)第一次过滤所产生的“滤渣”是_____(填化学式),过滤需要的玻璃仪器有__________(任写一种)。
(3)所得FeCO3需充分洗涤,检验是否洗净的方法是___________。第三次过滤所得到的“滤液”中存在的离子有_________(填离子符号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气的化学性质比较活泼,能支持燃烧,如图是木炭在氧气中燃烧实验示意图,对该实验分析并回答:
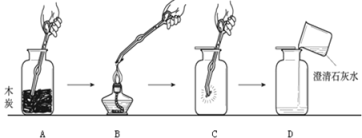
(1)从燃烧条件的角度分析,图B加热木炭的目的是______________。
(2)图B中熄灭酒精灯的方法是___________,原理是_____________。
(3)图C中木炭在氧气里燃烧比在空气里燃烧要剧烈,说明了_______________。
(4)图D在整个实验设计中的意图是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】往硝酸铜、硝酸银和硝酸镁的混合溶液中缓慢连续加入质量为mg的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是()
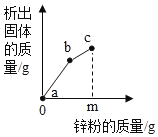
A.ab段(不含两端点)对应溶液中含有的金属离子的锌离子、银离子、镁离子
B.bc段(不含两端点)生成的金属是铜
C.c点对应溶液中含有的金属离子只有镁离子和锌离子
D.若ab段和bc段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,则m1>m2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学进行下图两个实验。
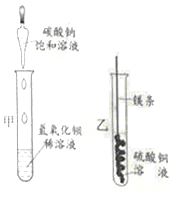
(l)甲实验中反应的化学方程式为____________;
(2)乙实验观察到的现象是___________,溶液由蓝色变成无色。
(3)把甲、乙反应后的溶液倒入同一烧怀,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
【查阅资料】硫酸钡不溶于酸。
【提出猜想】 白色沉淀为:Ⅰ._______;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为____________。 ②若______且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,________,猜想Ⅲ成立。 |
【拓展与思考】如果猜想Ⅲ成立,产生此结果的原因是做甲实验时___________;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空:
(1)金属活动性顺序表: K Ca Na___________Sn Pb(H) Cu Hg Ag Pt Au
(2)同学们选了三组物质来比较锌、铁、铜三种金属的活动性:
①Zn、Fe、 Cu、稀硫酸
②Fe、ZnSO4溶液、CuSO4 溶液
③ZnSO4溶液、FeSO4 溶液、Cu
仅用组内物质就能达到目的的是____________ (填序号)。
(3)用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如下图所示。试回答:
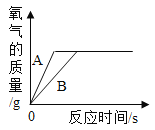
①曲线A表示的是____________(填“铁”或“锌”)跟稀硫酸反应的情况。
②上述曲线图除能说明①的结论外,还可得出的结论是(答一条)__________________。
(4)小明从实验废液中回收铜,得到的铜样品中含有少量铁粉,为测定样品中铜的质量分数,利用以下方案进行实验: ![]() ,将固体洗涤、干燥、称量为10.8g,请写出发生反应的化学方程式_____________________________,测得样品中铜的质量分数为__________________。
,将固体洗涤、干燥、称量为10.8g,请写出发生反应的化学方程式_____________________________,测得样品中铜的质量分数为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com