
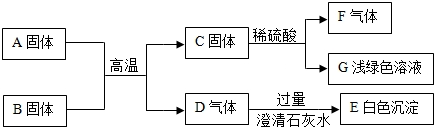
分析 根据A~F是初中化学常见物质,气体D能与澄清的石灰水反应生成白色沉淀E,所以E是碳酸钙,D是二氧化碳,G是浅绿色溶液,由固体C与硫酸反应生成,所以G是硫酸亚铁溶液,固体C和硫酸反应生成硫酸亚铁和气体F,所以C是铁,固体A、B在高温的条件下反应生成铁和二氧化碳,A是生活中常见的红色固体,所以A是氧化铁,B是碳,铁和硫酸反应生成硫酸亚铁和氢气,所以F是氢气,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1))A~F是初中化学常见物质,气体D能与澄清的石灰水反应生成白色沉淀E,所以E是碳酸钙,D是二氧化碳,G是浅绿色溶液,由固体C与硫酸反应生成,所以G是硫酸亚铁溶液,固体C和硫酸反应生成硫酸亚铁和气体F,所以C是铁,固体A、B在高温的条件下反应生成铁和二氧化碳,A是生活中常见的红色固体,所以A是氧化铁,B是碳,铁和硫酸反应生成硫酸亚铁和氢气,所以F是氢气,经过验证,推出的各种物质均满足题中的转化关系,推导正确,所以F是H2;
(2)依据图中的关系物质B具有的化学性质是还原性;
(3)生活中产生红色物质A的原因是:铁与空气中的氧气、水共同作用;
(4)通过推导可知,气体D是二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O.
故答案为:(1)H2;
(2)还原性;
(3)铁与空气中的氧气、水共同作用;
(4)Ca(OH)2+CO2=CaCO3↓+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


科目:初中化学 来源: 题型:解答题
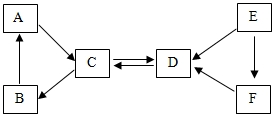 现有A~F六种常见物质,其中B是食品包装中的常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素,它们的转化关系如图.请回答:
现有A~F六种常见物质,其中B是食品包装中的常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素,它们的转化关系如图.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/(g) | 31 | 34 | 37 | 40.6 | 42 | 45.5 | 48 | 51 | 54 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气中含量最多的是氧气,氧气可支持燃烧 | |
| B. | 可以用木炭燃烧的方法测定空气中氧气的含量 | |
| C. | 过多排放二氧化碳,是造成温室效应的主要原因 | |
| D. | 空气有自净能力,排放到空气中的有害气体和烟尘不会对空气造成污染 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com