
 ×100%=40.9%,
×100%=40.9%,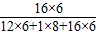 ×100%=x×
×100%=x× ×100%,
×100%,

科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 九年级小伟同学体检时得知缺维生素C(化学式为C6H8O6),校医开了一瓶维生素C,请小伟同学按说明书要求服用,五天一个“疗程”.
九年级小伟同学体检时得知缺维生素C(化学式为C6H8O6),校医开了一瓶维生素C,请小伟同学按说明书要求服用,五天一个“疗程”.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、维生素C含有碳、氢、氧三种元素 | B、维生素C是化合物 | C、维生素C中三种元素的原子个数比为6:8:6 | D、维生素C是由碳原子、氧原子、氢原子构成的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com