
分析 (1)根据质量守恒定律计算出二氧化碳的质量;
(2)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,结合二氧化碳的质量计算出碳酸氢钠的质量,再计算质量分数.
解答 解:(1)反应后生成的二氧化碳的质量为:13.6g+93g-100 g=6.6g;
(2)设参加反应的NaHCO3的质量为x
NaHCO3+HCl═NaCl+H2O+CO2↑
84 44
x 6.6 g
$\frac{84}{x}$=$\frac{44}{6.6g}$
x=12.6 g
小苏打样品中碳酸氢钠的质量分数为$\frac{12.6g}{13.6g}$×100%≈92.6%;
答:(1)完全反应生成二氧化碳的质量为6.6g;
(2)小苏打样品中碳酸氢钠的质量分数为92.6%.
点评 由于反应放出气体而使反应前后质量出现变化,可先使用质量守恒定律根据反应前后质量差计算出反应放出气体的质量,然后再利用气体的质量根据化学方程式计算出其它相关物质的质量.


科目:初中化学 来源: 题型:选择题
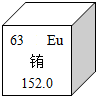 铕是一种稀土元素,如图是铕元素周期表中元素的相关信息,下列说法错误的是( )
铕是一种稀土元素,如图是铕元素周期表中元素的相关信息,下列说法错误的是( )| A. | 铕的原子序数是63 | B. | 铕属于非金属元素 | ||
| C. | 铕原子中的质子数是63 | D. | 铕的相对原子质量是152.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
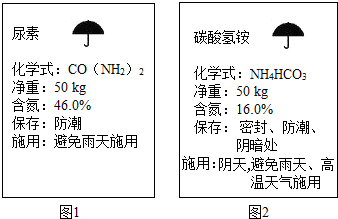
| A. | 只有②③④⑤ | B. | 只有①③④⑤ | C. | 只有①③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com